Sesión On_Line, celebrada el 18 de mayo de 2026 con la participación de:
María Victoria Zunzunegui, Damián Caballero y Pila4r Nogués.
Modera – Ramón Gálvez.

RESUMEN:
Madrid, 27 de marzo de 2026
La coalición PSOE más Sumar quiere convertir en secreto permanente el precio real pagado por cada medicamento cubierto por la sanidad pública. Y lo quiere hacer, además, sin debate y por la puerta de atrás.
Para conseguir este objetivo los grupos parlamentarios del PSOE y Sumar han presentado la enmienda 259 que se inserta como disposición final en el Proyecto de ley sobre Derechos de las Personas con Discapacidad. De esta manera no pasa por la Comisión de Sanidad del Congreso, que es donde debería debatirse, y se incrusta en una Ley con amplio consenso social, como es la discapacidad, hurtando de esta manera el debate necesario.
Desde la AAJM consideramos que el Ministerio de Sanidad debe rectificar de forma inmediata, y anular la introducción de esta enmienda en la ley. Este despropósito debe corregirse, impidiendo así, que el precio que se paga por un medicamento en España pase a ser secreto de Estado.

La coalición PSOE más Sumar quiere convertir en secreto permanente el precio real pagado
por cada medicamento cubierto por la sanidad pública. Y lo quiere hacer, además, sin debate y
por la puerta de atrás.
Para conseguir este objetivo los grupos parlamentarios del PSOE y Sumar han presentado la
enmienda 259 que se inserta como disposición final en el Proyecto de ley sobre Derechos de
las Personas con Discapacidad. De esta manera no pasa por la Comisión de Sanidad del
Congreso, que es donde debería debatirse, y se incrusta en una Ley con amplio consenso
social, como es la discapacidad, hurtando de esta manera el debate necesario.
Esta enmienda modifica el art.97.3 del RD Legislativo 1/2015 que protege la Información que
las empresas farmacéuticas proporcionan a la Administración. Pero la enmienda va más allá al
proteger también “los acuerdos de financiación que se alcancen, así como la información
derivada de las mismas o de su aplicación, incluyendo los precios de adjudicación de los
contratos de suministro de medicamentos que celebren las Administraciones Públicas, tendrán
carácter confidencial”. Es decir, no quieren que se conozca cuanto se paga por un
medicamento con nuestros impuestos.
El secretario de Estado de Sanidad lo justifica usando la aplicación del presidente Trump y sus
políticas trumpistas de la “Cláusula de la Nación más favorecida” (MFN) que obliga a que EEUU
no pague por un medicamento más que cualquier otro país del G7, además de Suiza y
Dinamarca”. Según el Sr. Padilla “la publicación del precio neto podría suponer una barrera al
acceso a los medicamentos innovadores” Aunque también reconoce que los estudios “sobre
posibles consecuencias de publicar el precio neto en España son difícilmente concluyentes” y
que la cláusula MFN supondrá “pequeños retrasos” en la incorporación de nuevos
medicamentos.
Lo que sí está claro es que esto supone un enorme retroceso en las políticas de transparencia
de cualquier Gobierno y el triunfo de la estrategia de la Industria farmacéutica contraviniendo
además lo que España votó en la OMS. La 72 Asamblea Mundial de la Salud aprobó una
resolución que instaba a los Estados Miembros de la OMS a publicar los precios que los
gobiernos pagan por lo medicamentos lo que contribuiría a precios más asequibles y ampliar el
ASOCIACIÓN POR UN ACCESO JUSTO AL MEDICAMENTO
2
Plaza de las cortes 11, planta 4ª https://accesojustomedicamento.org/
28014 Madrid accesojustomedicamentos@gmail.com
acceso a los medicamentos. Pero bueno, ya sabemos que EEUU se fue de la OMS y que España,
aunque no se vaya por lo que parece con esta decisión no hace caso.
Es curioso que esta enmienda se justifique invocando la capacidad negociadora del Estado y la
cláusula MFN, argumentos que lleva esgrimiendo la industria farmacéutica hace tiempo, y
además resulta aún más impactante y extraño que se haga con prisas cuando precisamente se
está pendiente la decisión judicial del Tribunal Supremo que pueden fijar doctrina sobre la
transparencia.
La posición del Ministerio con esta enmienda “progresista” es indistinguible de la posición de
la Industria. Este cambio tan importante y trascendente de la política del Ministerio merece
cuanto menos una explicación. Nos gustaría conocer si esta medida se debe amenazas de la
industria farmacéutica o bien a otro tipo de intereses.
Para esta Asociación, es desalentador comprobar que gobiernos teóricamente de izquierdas se
hacen indistinguibles en sus propuestas de gobiernos de orientación ultraliberal.
Consideramos que el MS debe rectificar de forma inmediata, y anular la introducción de esta
enmienda en la ley. Este despropósito debe corregirse, impidiendo así, que el precio que se
paga por un medicamento en España pase a ser secreto de Estado.
De dónde venimos, explica nuestra desagradable sorpresa
La Asociación por un Acceso Justo al Medicamento (AAJM) tiene como objetivo fundamental,
asegurar la accesibilidad y la asequibilidad a todos los ciudadanos y ciudadanas de los
medicamentos y vacunas necesarios para el mantenimiento y recuperación de la salud. Con
este motivo y dentro de la plataforma No Es Sano nos dirigimos a la ministra de Sanidad
Mónica García el 24 de noviembre de 2023 expresándole nuestro objetivo común con el resto
de las organizaciones que era y es mejorar la política farmacéutica y garantizar la
transparencia, la eficacia, la calidad, la accesibilidad y la asequibilidad de los medicamentos,
vacunas y de todas las tecnologías sanitarias en el Sistema Nacional de Salud (SNS).
Consideramos fundamental y así lo manifestábamos en la citada carta la necesidad de
“asegurar la transparencia en lo que se refiere a los costes de I+D en todas las etapas del
proceso de desarrollo y producción de medicamentos y tecnologías sanitarias, tal y como
recogen resoluciones recientes de la Asamblea de la Organización Mundial de la Salud y del
proceso de negociación y fijación de precios”.
Pensábamos y entonces creíamos compartir con el nuevo Ministerio de Sanidad (MS) del
Gobierno de España, en este caso de Sumar (Más Madrid), una posición próxima que
asegurara la transparencia y consiguiera precios justos y asequibles basados en los costes
reales, con márgenes de beneficios razonables.
ASOCIACIÓN POR UN ACCESO JUSTO AL MEDICAMENTO
3
Plaza de las cortes 11, planta 4ª https://accesojustomedicamento.org/
28014 Madrid accesojustomedicamentos@gmail.com
Desde 2022 hemos acudido en ocasiones sucesivas al Consejo de Transparencia y Buen
gobierno solicitando su posición activa instando al MS, información sobre precios de
medicamentos, financiados con fondos públicos ante la negativa a proporcionar los datos de
negociación y precios por sus sucesivos responsables. A lo largo de este periodo se han
producido sentencias previas de juzgados de lo contencioso administrativo que dieron la razón
a la petición, pero que posteriormente fueron rechazadas por la Audiencia Nacional. En el
momento actual está pendiente una resolución del Tribunal Supremo cuyo contenido podría
cambiar definitivamente la transparencia en la negociación de precios.
En este contexto nos produce asombro y consternación la posición adoptada recientemente
por el Ministerio de Sanidad y defendida por el secretario de Estado Javier Padilla, que supone
un giro de 180° en su postura anterior
Efectivamente, y como denuncia CIVIO el Ministerio de Sanidad desempeñado ahora por la
Coalición Sumar, con un teórico supuesto enfoque “progresista” dirigido a proteger los
derechos de la ciudadanía y a garantizar un acceso Justo y asequible a los medicamentos ha
tomado la decisión sorprendente enunciada en el incido de este comunicado; es decir, adoptar
los postulados de la industria farmacéutica y hurtar a la ciudadanía del conocimiento del
precio que se paga por medicamentos financiados públicamente.
Revista nº47 de Abril de 2026
• Las inaceptables maniobras de presión del gobierno de los EE. UU. sobre Zambia y el VIH. La táctica de negociación del Departamento de Estado de los EE.UU. para mantener la financiación del programa de VIH en Zambia es exigir a su gobierno el acceso a sus minerales críticos. Una maniobra tan vil que el director científico del programa global de VIH/SIDA renunció y lo llamó «un acuerdo que no podía soportar». {Global Trade Watch}. Un informe de la OCDE muestra que Big Pharma soborna rutinariamente a los prescriptores, reguladores de medicamentos, funcionarios gubernamentales y otros. Fuente Mad in America.
• Un comentario afortunado: Gollum en acción. El senador Ron Wyden de Oregón se refirió a la forma en que el fabricante de medicamentos AbbVie protege la exclusividad de su medicamento de enormes ganancias, Humira, comparando la manera en la que la empresa protege sus enormes ganancias con la forma en la que Gollum protege su anillo. Fuente CNBC.
• Un ejemplo corriente de un fármaco muy utilizado con un precio abusivo. Xtandi es un medicamento para el cáncer de próstata avanzado, comercializado por Astellas y Pfizer. El precio de Xtandi (enzalutamida) es exorbitante en EE.UU. 129.000 dólares al año, cerca de 90 dólares por cápsula. En España, el precio de Xtandi 40 mg es de 3.358,41 € (con IVA) por envase. (30 € aproximadamente la cápsula). Un fabricante canadiense ofrece enzalutamida genérica por 3 dólares la cápsula, una trigésima parte del precio del fabricante original (Esta referencia se encuentra incluida en el artículo que puede encontrarse en las páginas de este número: “Public Citizen sobre cómo hacer que los medicamentos sean más asequibles”).
Acuerdos que evitan la entrada de versiones genéricas y más baratas de Vyndamax en los EE. UU. hasta al menos el 1 de junio de 2031. Pfizer ha conseguido eliminar la competencia genérica, para su muy rentable y exitoso medicamento para el corazón Vyndamax (tafamidis) hasta el 1 de junio de 2031, mediante los acuerdos de liquidación con Cipla, Dexcel Pharma y Hikma Pharmaceuticals. Estos acuerdos, extienden la vida de la patente con una franquicia anual de más de 6 mil millones de dólares. Pfizer había calculado una disminución significativa en los ingresos a partir de de 2029. Con estos acuerdos, consigue mantener sus altos beneficios, desde 2028 hasta mediados de 2031. Su medicamento Vyndamax, utilizado para tratar la miocardiopatía amiloide de transtiretina (ATTR-CM), tiene alrededor de un 75% del volumen de prescripción actual en el mercado. Los acuerdos mencionados garantizan que los medicamentos cardíacos de alto rendimiento económico de Pfizer no se enfrenten a una competencia significativa en un futuro próximo, lo que permite a la compañía más tiempo para seguir con altos beneficios. Fuente Endpoints News. Un ejemplo más de la BigPharma, en este caso, el gigante Pfizer, de su estrategia de bloquear la entrada de genéricos para mantener beneficios escandalosos.
El secretario de Estado de Sanidad lanza una orden ministerial, para configurar una mesa para la participación de los pacientes, sin haber aún fijado el proyecto final de la Ley de participación. El día 17 de abril se publicó la Orden Ministerial para la constitución de la Mesa para la Participación de los pacientes. Esta Mesa, en la fluida retórica del secretario de Estado Javier Padilla, “supondrá el primer órgano a nivel estatal que desde el punto de vista de las instituciones públicas trabajará para garantizar la participación de las organizaciones de pacientes en los diferentes ámbitos de la Administración General del Estado en materia de sanidad, siendo un lugar de encuentro para todas las organizaciones de pacientes que trabajen a nivel estatal”. También nos advierte que esta Mesa es “la avanzadilla de la Ley de Organizaciones de pacientes actualmente en tramitación”. Cómo nuestras y nuestros lectores conocen la A AJM ha presentado alegaciones al mencionado proyecto (AJM Nº 46, marzo 2026 “Aportaciones de la AAJM al Anteproyecto de Ley de Organizaciones Pacientes”). Fuente Ministerio de Sanidad.
EDITORIAL. Revista nº47 de Abril de 2026
Soledad Cabezón Ruiz.
Presidenta de la AAJM.

En junio se cumplirán dos años desde que asumí la presidencia de la Asociación Acceso Justo al Medicamento, un honor tan ingente como lo es el compromiso de la asociación. Han sido dos años intensos, pero sobre todo marcados por una evolución preocupante: la política farmacéutica europea y española ha ido desplazándose, cada vez con mayor claridad, desde la defensa del medicamento como bien público hacia su consideración como activo estratégico industrial, económico y geopolítico. Lejos queda de aquella esperanza consensuada del Parlamento Europeo en 2027 de “reequilibrar el sector” donde el acceso a los medicamentos y la sostenibilidad de los sistemas sanitarios no quedase relegado y, menos aún, amenazada por la competitividad de la industria farmacéutica y, sobre todo, por los beneficios excesivos.
Desde la AAJM siempre hemos defendido una idea sencilla: los medicamentos, que se financian con dinero público en gran parte, deben responder al interés público, deben considerarse un bien social; la salud es un derecho entendido como básico por la ciudadanía, más allá de las regulaciones internacionales y nacionales. Eso significa precios justos, transparencia, rendición de cuentas, acceso equitativo y retorno social cuando la investigación, los ensayos, los datos y la infraestructura sanitaria han sido sostenidos por la ciudadanía.
Sin embargo, en estos años hemos visto avanzar una lógica distinta. Bajo el argumento de la competitividad, la innovación y la seguridad de suministro, aunque haciendo un uso indebido de la palabra acceso en los diferentes textos introductorios de la legislación reciente, se están consolidando marcos normativos que refuerzan el poder de la industria farmacéutica y debilitan la capacidad pública de control. La reforma farmacéutica europea se presenta como una modernización necesaria para mejorar el acceso, evitar desabastecimientos y acelerar la llegada de nuevos tratamientos, pero también explicita que uno de sus objetivos centrales es garantizar la competitividad de la industria farmacéutica europea.
No negamos que Europa necesite autonomía estratégica ni capacidad industrial. La pandemia mostró dependencias en medicamentos esenciales, principios activos y cadenas de suministro, pero autonomía sanitaria (industrial) no puede significar blindar rentas privadas, ampliar exclusividades, acelerar autorizaciones y proteger márgenes sin exigir transparencia, precios justos y retorno colectivo. Si lo público financia la investigación, sostiene hospitales, genera evidencia clínica y compra los medicamentos, lo público tiene derecho a saber cuánto paga, por qué lo paga y qué parte del valor creado vuelve a la sociedad.
Por eso resulta especialmente grave el retroceso en transparencia adoptado por el Gobierno de España, más por los partidos que sustentan al gobierno, con una manifiesta incoherencia con la posición mantenida a la fecha. La defensa reciente de la confidencialidad de los precios netos de los medicamentos financiados públicamente supone aceptar que la factura que pagamos entre todos pueda permanecer oculta. Se nos dice que revelar precios debilitaría la posición negociadora de España o podría retrasar el acceso a la innovación, pero la pregunta esencial sigue sin respuesta: ¿por qué debe sacrificarse la transparencia democrática para proteger estrategias comerciales privada? Una transparencia que se justifica por la defensa del sistema sanitario público, el derecho de los pacientes al acceso a la salud, a los medicamentos, amenazado con una factura farmacéutica imparable con precios de medicamentos que no se justifican por las inversiones en su desarrollo y, sin embargo, nos encontramos ante el sector industrial con mayor margen de beneficios a nivel europeo.
La industria farmacéutica lleva décadas justificando precios elevados en nombre del riesgo y del coste de la innovación. Pero ese relato es incompleto; no sólo porque la propia UE lo sitúa en torno al 17% del coste total del desarrollo, sino porque, además, una parte sustancial de la investigación biomédica se apoya en financiación pública, entre un 40 u 60%, según los estudios; universidades, hospitales, institutos de investigación y ensayos clínicos se realizan en sistemas sanitarios públicos; España es el principal país en desarrollo de ensayos clínicos en el sector público. La sociedad paga la ciencia, paga la infraestructura, paga los medicamentos y, además, se le pide que acepte no conocer el precio real. Ese modelo no es sostenible democráticamente, especialmente cuando año tras año, al menos, un 4% de la población reconoce no poder acceder a los tratamientos prescritos por razones económicas, no hay medicamentos para enfermedades cuya mortalidad amenaza con superar a la del cáncer en las próximas décadas, como son las infecciones por microrganismos resistentes, mientras sea mucho más lucrativo el sector oncológico.
A esta situación se suma un nuevo frente: el Espacio Europeo de Datos de Salud. Puede ser una herramienta disruptiva para mejorar la asistencia, la investigación y la seguridad sanitaria y, como he defendido públicamente, una oportunidad de garantía de sostenibilidad del sistema sanitario. Sin embargo, la regulación adoptada a nivel europeo hace que pueda convertirse en el mayor mercado integrado de datos sanitarios sensibles del mundo. Nuestra historia clínica, nuestros datos genéticos, nuestros diagnósticos, nuestros tratamientos y nuestra biografía biológica pueden pasar a ser una materia prima de enorme valor para farmacéuticas, tecnológicas, plataformas de inteligencia artificial y, potencialmente, modelos aseguradores o financieros.
La pregunta ya no es sólo cómo proteger la privacidad. La pregunta es quién monetizará nuestra salud. Si el ciudadano financia el sistema, aporta sus datos, participa en ensayos, paga impuestos y después compra colectivamente medicamentos a precios secretos, el contrato social sanitario empieza a romperse.
Estos dos años han confirmado la necesidad de la AAJM. Nuestra tarea es recordar, una y otra vez, que la innovación no puede ser una coartada para la opacidad; que la competitividad no puede estar por encima del derecho a la salud; que los datos sanitarios no pueden convertirse en una mina privada sin retorno público; y que los medicamentos financiados por la ciudadanía deben estar sometidos a control democrático.
Europa parece avanzar hacia una bioeconomía sanitaria en la que la salud se concibe cada vez más como sector tractor, mercado de datos, nicho tecnológico e infraestructura industrial. Ese camino puede generar avances, pero también enormes desigualdades si no se corrige su dirección. Frente a ello, la AAJM seguirá defendiendo un principio básico: la salud no puede organizarse como un mercado opaco donde la ciudadanía asume los costes y otros capturan los beneficios.
Nuestro objetivo sigue siendo claro: transparencia radical en precios y contratos; evaluación pública de costes reales de I+D; retorno social de la inversión pública; límites al abuso de monopolios; acceso equitativo a medicamentos esenciales; control democrático del uso secundario de datos sanitarios; y una política farmacéutica orientada al bien común, no a la maximización de beneficios.
Dos años después, la convicción es aún más firme. Sin transparencia no hay justicia. Sin justicia no hay acceso. Y sin acceso justo al medicamento, el derecho a la salud queda subordinado al negocio.
ORIGINAL. Revista nº47 de Abril de 2026
Fernando Lamata.
Presidente de la Comisión Editorial de la rAJM. Presidente de honor de la AAJM.
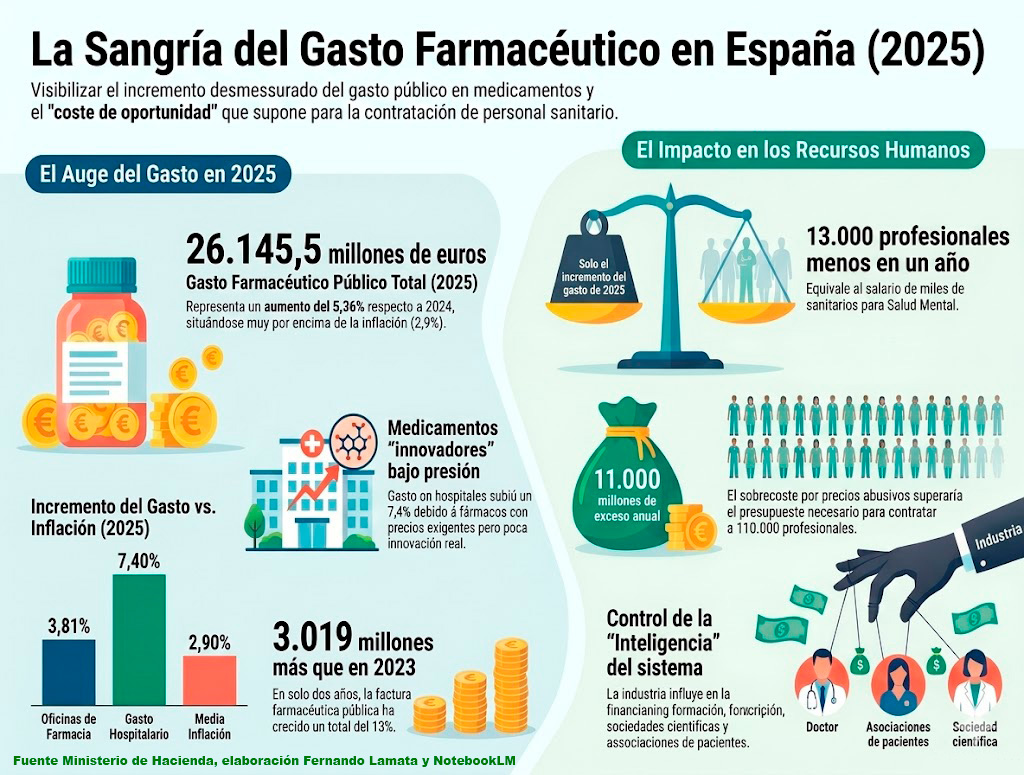
Según datos recientes del Ministerio de Hacienda, en el año 2025 el gasto farmacéutico público en España ascendió a 26.145,5 millones de euros (1). Esto supone 1.330,6 millones de euros más que en 2024 y un incremento del 5,36%. Solo ese incremento equivale a más de 13.000 profesionales que podrían haberse destinado, por ejemplo, a los programas de Salud Mental. Conviene recordar que el 50% de las personas que necesitan una consulta de salud mental tienen que recurrir a la sanidad privada por la falta de psiquiatras, psicólogos, trabajadores sociales y otros profesionales en la sanidad pública, y que la incidencia de problemas de salud mental se ha duplicado en los últimos diez años. El dinero que se gasta innecesariamente en precios excesivos de los medicamentos perjudica a los pacientes y a la sanidad pública.
El gasto en hospitales fue de 11.478,9 millones de euros, con un aumento del 7,4% respecto al año anterior, por la presión de los llamados “medicamentos innovadores” (que en muy pocas ocasiones suponen una innovación terapéutica efectiva real, pero que sistemáticamente exigen precios exagerados), mientras que en oficinas de farmacia fue de 14.675,6, con un aumento del 3,81% respecto al año anterior. Ambas cifras por encima de la inflación que se situó en el 2,9%.
Mirando un año más atrás, respecto a 2023 el gasto farmacéutico público en 2025 ha aumentado en 3.019 millones de euros, un 13%. Equivale a más de 30.000 puestos de trabajo de profesionales sanitarios. Si comparamos en euros constantes, el incremento real es de un 6,7%. Sigue siendo importante. Y si ajustamos por habitante, todavía se aprecia un incremento del 4,6% entre 2023 y 2025.
Yendo todavía un poco más atrás vemos que en 2021 el incremento de gasto farmacéutico fue del 7% respecto al año anterior; en 2022 del 3,8%, en 2023 de 5,3% y en 2024 fue del 7,3%. Como vemos es una sangría constante para el Sistema Nacional de Salud.
Conviene insistir: el exceso actual de gasto farmacéutico público, por precios abusivos, muy por encima de los costes de fabricación y de investigación, supera los 11.000 millones anuales en la factura farmacéutica. El objetivo del Gobierno central y los Gobiernos autonómicos debería ser una reducción progresiva de ese exceso de gasto, acercando los precios actuales a los precios cercanos al coste real de fabricación e investigación. Por otra parte, la presión de marketing de la industria se traduce en una sobre prescripción, y un consumo de medicamentos innecesarios, que se estima en un 20-30% del total. El hecho de que la factura farmacéutica siga aumentando año a año supone un factor de riesgo e inestabilidad para el Sistema Nacional de Salud.
Además de tomar conciencia de ese exceso de gasto (que serviría, por ejemplo, para contratar a más de 110.000 profesionales sanitarios y reducir significativamente las listas de espera, aumentando el tiempo de atención a cada paciente), conviene saber que la industria farmacéutica, con parte de esos beneficios, financia la formación continuada de los médicos, las sociedades científicas, las revistas médicas, así como las guías clínicas, congresos médicos, cátedras de patrocinio, etc., etc., orientando así la prescripción hacia sus productos. Parte de esos beneficios se destinan a acciones de lobby para influir en los gobiernos y parlamentos, nacional, autonómicos y europeo, con el objetivo de lograr legislaciones, normativas y decisiones sobre precios que les favorezcan. Parte de esos beneficios se destinan a financiar asociaciones de pacientes, condicionando así sus posiciones y manifestaciones. Y parte de esos beneficios excesivos se destinan, a través de empresas intermediarias, a controlar la información sobre consumo de medicamentos, y diversa información clínica e institucional. Podríamos decir que la industria farmacéutica controla “la inteligencia” del Sistema Nacional de Salud.
Por eso es urgente diseñar una política farmacéutica de Estado que contribuya a cambiar esta tendencia y recupere estos recursos públicos para que sean utilizados en beneficio de la población. Así mismo, esta nueva política farmacéutica debería lograr que las Autoridades Sanitarias recuperen la “inteligencia” del sistema, evitando la presión de la industria sobre profesionales, pacientes y administraciones públicas, y permitiendo así la toma de decisiones independiente.
(1) Ministerio de Hacienda. Indicadores sobre gasto farmacéutico y sanitario. Consultado en 1 abril 2026. https://www.hacienda.gob.es/eu-ES/CDI/Paginas/EstabilidadPresupuestaria/InformacionAAPPs/Indicadores-sobre-Gasto-Farmac%C3%A9utico-y-Sanitario.aspx
ORIGINAL. Revista nº47 de Abril de 2026
Javier Sánchez Caro.
Presidente de la Comisión de Bioética de Castilla-La Mancha. Vocal de la Junta Directiva de la AAJM.
1.- Introducción
El anteproyecto de Ley de las Organizaciones de Pacientes, que ha sido sometido recientemente a información pública, tiene como objetivo declarado reforzar dichas organizaciones de ámbito estatal en su papel de interlocutoras ante la Administración General del Estado, garantizar su participación, definir las medidas de fomento que los poderes públicos puedan aportar en su beneficio y desarrollar los derechos y las obligaciones que les corresponden.
En su Exposición de Motivos recuerda la participación comunitaria recogida en la Ley General de Sanidad (1986), en la Ley de Cohesión y Calidad (2003) y en la Ley General de Salud Pública (2011), haciendo a continuación una breve referencia histórica de dichas organizaciones en nuestro País y en Francia, Reino Unido, Alemania y, a nivel supranacional, en la Agencia Europea del Medicamento.
Las organizaciones de pacientes se rigen por la Ley Orgánica reguladora del Derecho de Asociación (2002) y su papel específico en el ámbito sanitario está reconocido por la Ley Básica de Autonomía del Paciente (2002).
Parece evidente que la única forma de colocar al paciente en el centro, tal y como se afirma constantemente (principio de autonomía, información, consentimiento informado), es escucharlo, oír su voz, pero algo que parece sencillo puede no serlo tanto en determinadas ocasiones, dados los conflictos de interés que pueden existir en el seno de las organizaciones y a los que nos referiremos posteriormente.
Las asociaciones de pacientes, en España alrededor de 1900, atadas generalmente a una enfermedad, son necesarias para el buen funcionamiento de la asistencia sanitaria, que ha sufrido profundas modificaciones en los últimos tiempos, y cumplen diversas finalidades, además de la ya mencionada de su participación en las políticas públicas sanitarias: representan los intereses de las personas en relación con su enfermedad, humanizan la asistencia, promueven el bienestar físico, emocional y social y contribuyen a la educación sanitaria en su ámbito de actuación (principio de beneficencia); son claves en la investigación y evaluación de tratamientos, cuidando de que la atención sea segura y de calidad, de manera que se evite el dolor y el sufrimiento innecesario (no maleficencia); procuran, en fin, que se mantenga la equidad, eliminando todo tipo de barreras (principio de justicia). Además, su fuerza e importancia se amplía cuando se integran en plataformas integradoras, tal y como en Europa la European Patiens’Forum o, en España, la Plataforma de Organizaciones de Pacientes o el Foro Español de Pacientes.
El Anteproyecto de Ley citado asume la razonable idea de que es necesario regular su actuación en virtud de su singularidad, pues de otra manera no se reconocería la importancia de las organizaciones formadas por pacientes, familiares o personas cuidadoras de los mismos, además de que no existen instrumentos que sirvan de censo para encauzar su participación.
Se trata de un proyecto normativo que reduce su ámbito de actuación a las asociaciones, federaciones, confederaciones y uniones de ámbito estatal, siempre que desarrollen sus funciones en más de una comunidad o ciudad autónoma y a las que se exige, entre otros principios, actuar de modo transparente y rendir cuentas, incluyendo las fuentes de financiación tanto públicas como privadas. Desde el punto de vista de los derechos, pueden acceder a financiación pública mediante convocatoria de ayudas, subvenciones o convenios, entre otros, diseñados con criterios objetivos y transparentes, sin incrementar el gasto público.
La normativa se basa en la potestad de autoorganización de la Administración General del Estado y circunscribe su aplicación, por tanto, al ámbito de ésta y de su sector público institucional, con excepción del concepto (art-2), los principios rectores (art-4) y los órganos de participación estatal (art-9), que se dictan al amparo de la Constitución, que atribuye al Estado la competencia en materia de bases y coordinación general de la sanidad, a lo que hay que añadir la modificación que se lleva acabo de la ley de Cohesión y Calidad (Disposición final primera).
No ha considerado el Anteproyecto efectuar regulación alguna a los posibles conflictos de interés que pueden plantearse con ocasión del normal funcionamiento de las organizaciones y las referencias a su financiación, tal y como han que dado expuestas, deben en consecuencia considerarse insuficientes. Es conocido que, hasta la fecha, no existe regulación alguna sobre esta materia y el legislador potencial, en el Anteproyecto que ahora se comenta, ha desperdiciado la ocasión que se le presentaba para sentar las bases sobre esta materia, estableciendo estrictos mecanismos para evitar conflictos de interés, fraude y corrupción, incluyendo la cumplimentación de declaraciones de ausencia de conflicto de interés, todo ello con la finalidad de garantizar la independencia en la toma de decisiones. Por el contrario, la norma proyectada apela a las organizaciones para que sean ellas las que adopten las medidas de prevención y gestión de conflictos de intereses que resulten oportunas, lo que no parece adecuado a la vista de lo que ha venido sucediendo en este sector (artículo 4.g)
2.- Financiación de las asociaciones
Las fuentes de financiación tienen un origen variado y su procedencia es tanto pública como privada. En concreto, se reducen a las cuotas de los socios, las donaciones privadas, los fondos públicos- vía subvenciones estatales, autonómicas o locales- y las provenientes de la industria farmacéutica, que es la financiación más sensible desde el punto de vista ético, hasta el punto de que las asociaciones vienen reclamando que la ley garantice una financiación pública estable que reduzca la dependencia de la industria privada y asegure su supervivencia como agentes sociales independientes.
Para garantizar la independencia y la transparencia necesarias existen normas y recomendaciones de diferente origen. Fuera de nuestras fronteras, la European Medicines Agency ha establecido reglas estrictas de conflicto de interés en la participación de los pacientes; la Health Action Internacional ha denunciado riesgos de dependencia de la industria y el código EFPIA, de la industria farmacéutica europea, ha regulado la relación con las asociaciones de pacientes.
En España, como hemos señalado en otra ocasión (“Conflictos de intereses y salud”, Boletín de Derecho Sanitario y Bioética n.º 232, marzo 2025, Servicio de Salud de Castilla-La Mancha), el marco regulatorio abarca la legislación general sobre transparencia y subvenciones y los códigos de autorregulación, entre los que destaca el código de buenas prácticas de Farmaindustria, que obliga a declarar las transferencias de valor a las asociaciones y a formalizar convenios por escrito, y el código de conducta de la Plataforma de Organizaciones de Pacientes, además de otras iniciativas, como la publicación de ayudas en webs corporativas o las recomendaciones del Ministerio de Sanidad.
3.- Situación actual de los pagos de las farmacéuticas a las organizaciones de pacientes en España
Veintiún organizaciones de pacientes concentran la mitad de los pagos de las farmacéuticas en España (Manuel Rico y Chris Matthews, “Precios mortales”, Investígate Europe, 17 de septiembre de 2024).
La industria financió en 2022, con 7,88 millones, a las asociaciones españolas de pacientes. Recibieron dinero 349 entidades, pero sólo 21 obtuvieron más de 100.000 euros. Y, en conjunto, se llevaron 3,93 millones, lo que supone la mitad del total.
La financiación de las asociaciones de pacientes, “transferencias de valor según la industria”, es la menos conocida y la menos cuantiosa, a diferencia de la que llevan a cabo para actividades de formación a miles de profesionales sanitarios, o de las que patrocinan a sociedades científicas y asociaciones médicas, que son mucho más importantes y de las que no nos ocupamos en esta ocasión. Todas ellas salen de los enormes beneficios de las farmacéuticas.
Las diez organizaciones de pacientes españolas que más dinero recibieron son las siguientes, expresado en euros: Plataforma de Organizaciones de Pacientes (310.569), se trata de una cantidad que representa el 68% de todos los ingresos de la plataforma; Grupo Español de Pacientes con Cáncer (275.945); Asociación Española de Afectados por Linfoma, Mieloma y Leucemia (250.938); Asociación Esclerosis Múltiple (236.072); Asociación Psoriasis (232.347); Coordinadora Estatal de VIH y Sida (232.020); Asociación Española contra el Cáncer (231.907); Federación Española de Diabetes (200.130); Federación Española de Enfermedades Raras (195.025) y Comunidad Española de Pacientes con Mieloma Múltiple (188.327).
En el marco europeo, según el trabajo citado, las entidades españolas ocupan el sexto lugar de las que más dinero recibieron, lo que corresponde con el peso de nuestra población. Además, la financiación por patologías es semejante a la europea, pues las que más dinero recibieron se refieren a seis áreas: cáncer, esclerosis múltiple, VIH/sida, diabetes, enfermedades raras y dolencias cardíacas.
Soledad Cabezón, presidenta de la Asociación Acceso Justo al Medicamento, entrevistada en el trabajo referido, reconoce la importancia de las organizaciones de pacientes: “realizan una tarea fundamental ya que cubren una serie de servicios de los que no se encarga la sanidad pública: de prestaciones a los pacientes, de sensibilización, de otorgar visibilidad a las enfermedades”. Y añade “tienen una gran capacidad de influencia en temas muy sensibles para la industria, como la decisión de financiar públicamente un medicamento o no”. Afirma, además, “que la sociedad no es consciente de que una parte de la financiación de las organizaciones de pacientes se la dan las empresas farmacéuticas”. En resumen, entiende que es necesaria una regulación para impedir la influencia desmedida de las farmacéuticas.
Del panorama expuesto en relación con las asociaciones, y la consiguiente financiación de la industria, se aparta de manera excepcional la organización Salud Mental España, una confederación que cuenta con 60.000 socios individuales, 340 asociaciones y 18 federaciones. En su código ético se dice lo siguiente: “Salud Mental España expresa su compromiso de no desarrollar actividades con industrias farmacéuticas que supongan la obtención directa de financiación”. La entidad se compromete a colaborar con empresas sólo “en actividades que supongan la difusión de la visión de la Confederación, el respeto del enfoque de derechos y la promoción de la salud mental”. Tal enfoque se adoptó tras un intenso debate y para evitar los conflictos de interés. En la actualidad, el 66% de sus ingresos tienen procedencia pública, aunque en algún momento de su historia la financiación de la industria llegó a suponer el 40% de los ingresos totales.
4.- Los conflictos de interés en las organizaciones de pacientes
Los conflictos de interés entre asociaciones de pacientes y la industria farmacéutica en España surgen principalmente por la dependencia económica de estas entidades de las farmacéuticas, lo que puede influir en su posicionamiento sobre políticas sanitarias, acceso a medicamentos o priorización de tratamientos. Esta relación genera riesgos para la independencia y la equidad del Sistema Nacional de Salud (SNS), por ejemplo, cuando las asociaciones de pacientes reciben fondos de la industria, priorizando intereses comerciales sobre los de los usuarios, como los que resultan de presionar para acceder a fármacos caros, sin cuestionar, precios o eficacia
La financiación de las asociaciones de pacientes es un tema crítico que busca equilibrar la necesidad de recursos para funcionar con la exigencia ética de independencia, transparencia y sostenibilidad. En España, el debate actual se centra el regular estas fuentes de ingresos públicas y privadas para garantizar que la actividad de estas organizaciones se desarrolla de manera ética, sin que la industria farmacéutica ejerza control sobre sus contenidos. Sin embargo, el anteproyecto que comentamos no ha abordado esencialmente este problema, al no contemplar la cuestión clave de los conflictos de interés, apelando únicamente a la buena voluntad de las asociaciones, tal y como venimos exponiendo.
En 2020, un dictamen parlamentario intentó prohibir la financiación directa o indirecta, pero generó alarma por la dependencia económica de las asociaciones, lo que abocaba a su extinción en la mayor parte de los casos. En todo caso, además de la transparencia, rendición de cuentas, códigos éticos y auditorías externas, que tendrá que desarrollarse reglamentariamente, debe garantizarse la independencia económica de las organizaciones, habiéndose planteado en alguna ocasión, por ejemplo, limitar en un porcentaje moderado la financiación de la industria en un 20% como máximo. Como opina Fernando Lamata, “la independencia económica de las asociaciones sería fundamental para garantizar que sus opiniones no estén mediadas por la presión de sus financiadores. Si no, correrían el riesgo de ser utilizadas como agentes comerciales de la industria dentro de los órganos de toma de decisión de la Administración, que debe representar los intereses de toda la sociedad”.
5.- La posición de la AAJM (Revista de la Asociación. nº 46, marzo 2026)
A la vista de las consideraciones anteriores, sobre la base de que el anteproyecto no ha efectuado una regulación de los conflictos de intereses, la Asociación por el Acceso Justo al Medicamento ha trasladado al Ministerio de Sanidad una serie de aportaciones, que se contienen en la Revista mencionada, y que ahora, en síntesis, se transcriben de la siguiente manera:
“Para preservar su independencia, debe establecerse la prohibición de que las organizaciones de pacientes reciban ingresos de empresas farmacéuticas o biotecnológicas. Asimismo, los miembros y representantes de estas organizaciones tampoco podrán recibir ningún estipendio de esas empresas, ni directa ni indirectamente.
La Administración General del Estado facilitará a las organizaciones de pacientes, una financiación suficiente”.
ORIGINAL. Revista nº47 de Abril de 2026
Juan Luis Beltrán Aguirre.
Presidente del Consejo de Transparencia de Navarra.

I. Sobre los procesos judiciales donde se debate la publicidad o confidencialidad del precio de los medicamentos de financiación pública
Como es bien conocido, en la gestión pública del medicamento se enfrentan, de un lado, el principio de transparencia, que garantiza un control público de su gestión, la rendición de cuentas, así como prevenir y detectar corruptelas, y de otro lado, los intereses económicos y comerciales de la industria farmacéutica, que para protegerlos demanda la mayor opacidad y confidencialidad posible en todos los ámbitos del medicamento en los que interviene: investigación, fabricación, autorización, fijación del precio, compra de medicamentos por las Administraciones sanitarias autonómicas.
En el ámbito legislativo, este conflicto entre los dos bienes jurídicos enfrentados, transparencia/opacidad, lo encontramos en el Real Decreto Legislativo 1/2015, de 24 de julio, por el que se aprueba el Texto Refundido de la Ley de Garantías y Uso Racional de los Medicamentos y Productos Sanitarios (TRLGURM) y en la Ley 19/2013, de 9 de diciembre, de Transparencia, Acceso a la Información Pública y Buen Gobierno (LTAIBG). Así, el artículo 7 del TRLGURM establece que Las administraciones sanitarias garantizarán la máxima transparencia en los procesos de adopción de sus decisiones en materia de medicamentos. A pesar de esta declaración general de transparencia, en el artículo 97.3 se matiza al establecer que la información sobre los aspectos técnicos, económicos y financieros que obtenga la Administración General del Estado de los laboratorios farmacéuticos será confidencial. Por su parte, la LTAIBG, en su disposición adicional primera, apartado 2, establece: 2. Se regirán por su normativa específica, y por esta Ley con carácter supletorio, aquellas materias que tengan previsto un régimen jurídico específico de acceso a la información, y en su artículo 14.1, con el objeto de preservar determinados valores que considera prevalentes respecto de la transparencia, establece diversas limitaciones al derecho de acceso a la información pública que enumera.
El Ministerio de Sanidad y la industria farmacéutica esgrimen en favor de la opacidad que el TRLGURM contiene un régimen específico de acceso a la información que, en virtud de la citada disposición adicional primera, desplaza y hace inaplicable la LTAIBG, y que ese régimen garantiza la confidencialidad de los precios fijados, y que para el supuesto de que se considere aplicable la LTAIBG, subsidiariamente, respecto del precio de los medicamentos de financiación pública, son aplicables los límites al acceso de información establecidos en el artículo 14.1 LTAIBG, letra h) Los intereses económicos y comerciales, y letra k) La garantía de la confidencialidad o el secreto requerido en procesos de toma de decisión.
Tres entidades privadas sin fin de lucro, la Fundación Ciudadana Civio, la Fundación Salud por Derecho y la Organización de Consumidores y Usuarios, vienen reclamando transparencia por parte de la Administración sanitaria en la gestión del medicamento y, por ende, se haga público el precio de financiación pública de los medicamentos. A partir del año 2022 decidieron adoptar una actitud más beligerante realizando concretas actuaciones tendentes a conseguir que la transparencia respecto del precio fijado para los medicamentos sea una realidad.
Así, con amparo en la LTAIBG, presentaron escritos ante el Ministerio de Sanidad formulando solicitudes de acceso a información relativa al precio de diversos medicamentos innovadores (Luxturna, Zolgensma, Yescarta, Remdesivir, Lamadelumab, etc.) y su impacto en el presupuesto sanitario. El Ministerio de Sanidad sistemáticamente negó el acceso a esta información alegando que son datos que tienen la consideración de confidenciales conforme al artículo 97.3 del TRLGURM y 14.1, letras h y k, de la LTAIBG. Ante esta negativa, la Fundación Ciudadana Civio y la Fundación Salud por Derecho formularon respectivas reclamaciones ante el Consejo de Transparencia y Buen Gobierno (CTBG), que, decantándose plenamente por la prevalencia de la transparencia, estimó todas las reclamaciones instando al Ministerio de Sanidad a que facilite a las entidades reclamantes los datos solicitados.[I]
No conformes con las resoluciones del CTBG favorables a la transparencia, el Ministerio de Sanidad y los laboratorios farmacéuticos implicados (Gilead, Tekeda y Novartis) interpusieron recursos contencioso-administrativos contra cada una de esas resoluciones del CTBG pretendiendo que ha de prevalecer la confidencialidad de la información que habían solicitado las Fundaciones y que procedía anular las citadas resoluciones del CTBG.
Por falta de espacio y por no cansar al lector, pues son ocho los procedimientos judiciales, voy a relatar seguidamente los procesos judiciales que actualmente han llegado al Tribunal Supremo en recurso de casación.
a) Convenio vacunas de Biontech/Pfizer
Un ciudadano presentó una solicitud de acceso a una copia del Convenio entre el Ministerio de Sanidad y el Gobierno de Andorra, sobre la reventa de vacunas de Biontech/Pfizer para luchar contra la emergencia sanitaria provocada por el virus de SARS-CoV-2. El Ministerio entregó determinada información que el solicitante consideró insuficiente, lo que motivó que formulara una reclamación ante el Consejo de Transparencia y Buen Gobierno, que la estimó por Resolución 832/2021, de 8 de abril de 2022. Interpuesto recurso contencioso-administrativo por la Agencia Española de Medicamentos y Productos Sanitarios, el Juzgado Central de lo Contencioso Administrativo número uno, por Sentencia 58/2023, de 25 de marzo de 2023, desestima el recurso y confirma la resolución del CTAIBG. Interpuesto recurso de apelación por la Agencia Española de Medicamentos, la Sección Séptima de la Audiencia Nacional, en Sentencia de 25 de junio de 2024, estima el recurso de apelación y anula la Sentencia del Juzgado Central. Finalmente, interpuesto recurso de casación por el Consejo de Transparencia y Buen Gobierno, es admitido a trámite por Auto del Tribunal Supremo de 29 de enero de 2025, y por Sentencia 301/2026, de 11 de marzo de 2026, estima el recurso de casación y casa la sentencia de apelación. En respuesta a las cuestiones de interés casacional, el TS razona que la regulación establecida en el Reglamento (CE) nº 1049/2001 del Parlamento Europeo y del Consejo, relativo al acceso público a los documentos del Parlamento Europeo, del Consejo y de la Comisión, no es aplicable a los documentos que obren en poder de la Administración de un Estado miembro, y que el acceso a la información ha de resolverse aplicando la normativa nacional, y que, en este caso, la Agencia Española de Medicamentos y Productos Sanitarios no ha justificado suficientemente la concurrencia del límite del art. 14.1.k) LTAIBG -la garantía de confidencialidad o el secreto requerido en procesos de toma de decisión-, que tiene un alcance temporal limitado, no teniendo incidencia en el proceso de negociación una vez el acuerdo ya ha sido alcanzado, y que tampoco se ha justificado el límite del art. 14.1.c) LTAIBG -perjuicio a las relaciones exteriores- pues, afirma la Sentencia, “La intervención de un tercer Estado en la elaboración de un convenio no implica que su contenido deba ser secreto o que la información referente al mismo pueda ser denegada invocando genéricamente el posible daño a las relaciones exteriores…»
b) Medicamento Luxturna desarrollado por Novartis
La Fundación Ciudadana Civio solicitó al Ministerio de Sanidad información sobre el precio de ese medicamento. El Ministerio denegó la información. Interpuesta reclamación ante el CTBG, por Resolución 1076/2021, de 15 de junio de 2022, estima la reclamación formulada por la Fundación Ciudadana Civio relativa a las condiciones de financiación y precio del medicamento y requiere al Ministerio de Sanidad que la facilite. Interpuesto recurso contencioso-administrativo por el Ministerio de Sanidad y Novartis (procedimiento ordinario 36/2022 seguido en el Juzgado Central nº 9) el Juzgado Central, por Sentencia 117/2023, de 11 de julio de 2023, desestima las demandas presentadas y confirma la resolución del CTBG. Novartis y el Ministerio de Sanidad presentan sendos recursos de apelación ante la Audiencia Nacional contra esta Sentencia. La Audiencia Nacional, por Sentencia 4550/2025, de 23 de abril de 2025, estima los recursos de apelación acumulados y considera que el art. 97.3 del TRLGURM, configura un régimen legal de confidencialidad que opera con carácter preferente frente a la LTAIBG. A juicio de la Sala, la divulgación del precio financiado y de las condiciones asociadas permitiría inferir datos estratégicos sobre costes, márgenes y esquemas de negociación, lo que comprometería tanto los intereses comerciales de las compañías como la posición negociadora del propio Sistema Nacional de Salud. Interpuesto por el Consejo de Transparencia y Buen Gobierno y por la Fundación Ciudadana Civio recurso de casación ante el Tribunal Supremo, es admitido a trámite por Auto de 17 de diciembre de 2025. En el momento de escribir este artículo el TS no ha dictado Sentencia de casación.
c) Medicamento Zolgensma desarrollado por Novartis
– La Fundación Ciudadana Civio solicitó al Ministerio de Sanidad información sobre el precio de ese medicamento. El Ministerio denegó la información. Interpuesta reclamación ante el CTBG, por Resolución de 22 de diciembre de 2022, estima la reclamación formulada por la Fundación Ciudadana Civio relativa a las condiciones de financiación y precio del medicamento. Interpuesto recurso contencioso-administrativo por el Ministerio de Sanidad y Novartis (procedimiento ordinario 2/2023 seguido en el Juzgado Central nº 4), el Juzgado, por Sentencia 110/2023, de 6 de septiembre de 2023, desestima las demandas presentadas y confirma la resolución del CTBG. Novartis y el Ministerio de Sanidad presentan recurso de apelación contra esta Sentencia. La Audiencia Nacional, por Sentencia de 23 de abril de 2025, estima el recurso de apelación con similar argumentación que la Sentencia de Luxturna. Interpuesto por la Fundación Ciudadana Civio recurso de casación ante el Tribunal Supremo, es admitido a trámite por Auto de 20 de noviembre de 2025. En el momento de escribir este artículo el TS no ha dictado Sentencia de casación.
– La Fundación Salud por Derecho y la Organización de Consumidores y Usuarios solicitaron al Ministerio de Sanidad información sobre el precio de ese medicamento. El Ministerio denegó la información. Interpuesta reclamación ante el CTBG, por Resolución de 28 de marzo de 2023, estima la reclamación formulada por la Fundación Salud por Derecho y la Organización de Consumidores y Usuarios, relativa a las condiciones de financiación y precio del medicamento. Interpuesto recurso contencioso-administrativo por el Ministerio de Sanidad y Novartis ante la Audiencia Nacional [II], por Sentencia de 23 de abril de 2025, estima el recurso contencioso-administrativo con similar argumentación que la Sentencia de Luxturna. Interpuesto por la Fundación Salud por Derecho, la Organización de Consumidores y Usuarios y el CTBG recurso de casación ante el Tribunal Supremo, también es admitido a trámite -recurso núm. rca/0001464/2026-. En el momento de escribir este artículo el TS no ha dictado Sentencia.
La Audiencia Nacional, en sus sentencias de apelación, considera que el artículo 97.3 del TRLGURM, al declarar confidencial la información técnica, económica y financiera aportada por los laboratorios en los procedimientos de fijación de precios, establece un régimen legal específico que opera con preferencia sobre la Ley de Transparencia, quedando esta como supletoria. Argumenta que facilitar el acceso a la información comprometería la confidencialidad garantizada por el artículo 97.3 del TRLGURM, ya que el conocimiento combinado del precio industrial y del precio financiado permitiría inferir datos estratégicos sobre costes, márgenes y condiciones de negociación, esenciales para salvaguardar la posición negociadora del Sistema Nacional de Salud en un mercado internacional competitivo.
Las sentencias dictadas en apelación pueden ser recurridas en casación ante el TS. La casación no es una tercera instancia. El TS solo admite el recurso cuando aprecia que el asunto plantea una cuestión jurídica con interés casacional objetivo para la formación de jurisprudencia y potenciar la seguridad jurídica. La sentencia de casación fija la interpretación de aquellas normas sobre las que, en el auto de admisión a trámite, se consideró necesario el pronunciamiento del TS y resuelve las cuestiones y pretensiones deducidas en el proceso, anulando la sentencia recurrida, en todo o en parte, o confirmándola. Desde esta perspectiva, el TS justifica la admisión a trámite de los recursos de casación respecto de los medicamentos Luxturna y Zolgensma a fin de sentar doctrina jurisprudencial sobre tres aspectos clave: primero, si la normativa farmacéutica configura un régimen específico de acceso a la información que desplace la aplicación de la LTAIBG; segundo, si la reserva de confidencialidad del artículo 97.3 TRLGURM se limita a la información facilitada por los laboratorios o alcanza también al precio financiado y a las condiciones de financiación; y tercero, si esa confidencialidad se limita al proceso decisorio mientras está en curso o se extiende en el tiempo una vez adoptada la decisión.
II. Sobre las tres cuestiones de interés casacional que plantea el TS
Seguidamente, doy respuesta, según mis conocimientos jurídicos, a las tres cuestiones de interés casacional sobre las que ha de pronunciarse el TS.
Primera. Si la normativa del TRLGURM configura un régimen específico de acceso a la información que desplace la aplicación de la LTAIBG.
El TS se ha pronunciado en diversas sentencias (por todas, sentencia de 11 de junio de 2020 -Recurso de Casación 577/2019-) sobre el alcance de la disposición adicional primera de la LTAIBG afirmando que para ser aplicable es imprescindible que las normas sectoriales contengan un sistema alternativo y completo de regulación específica de acceso a la información que excluya totalmente la aplicación de la LTAIBG. La norma sectorial debe diseñar un régimen de acceso completo -con su sujeto activo y pasivo, límites, procedimiento a seguir, etc.-. En concreto, la Sentencia del TS de 8 de marzo de 2021 -Recurso de Casación 1975/202-, que analizaba la solicitud de información sobre la autorización de un medicamento, sienta en su fundamento tercero, titulado “Sobre el alcance de la disposición adicional primera de la Ley de Transparencia”, las siguientes consideraciones:
“Debemos ahora avanzar en la determinación del alcance de la disposición adicional primera, apartado segundo, de la Ley de Transparencia, precisando qué debemos entender por un régimen específico alternativo y cómo opera la supletoriedad de la Ley de Transparencia. Así, hemos de aclarar, en primer lugar, que sin duda hay un régimen específico propio cuando en un determinado sector del ordenamiento jurídico existe una regulación completa que desarrolla en dicho ámbito el derecho de acceso a la información por parte, bien de los ciudadanos en general, bien de los sujetos interesados. En tales supuestos es claro que dicho régimen habrá de ser aplicado con carácter preferente a la regulación de la Ley de Transparencia, que en todo caso será de aplicación supletoria para aquellos aspectos que no hayan sido contemplados en tal regulación específica siempre, claro está, que resulten compatibles con ella. En este sentido, conviene subrayar que, en contra de lo que se ha alegado en ocasiones, la existencia de un régimen específico propiamente tal no excluye la aplicación supletoria de la Ley de Transparencia. La disposición adicional primera dispone literalmente lo contrario, tanto en el apartado 2 como en el tercer apartado, que se refiere de forma expresa al carácter supletorio de la Ley de Transparencia en el sector medioambiental, que tiene un régimen específico de acceso a la información de rango legal en la Ley 27/2006, de 18 de julio.”
Pues bien, aplicando esa doctrina al caso que nos ocupa es evidente que la regulación específica contenida en el artículo 97.3 del TRLGURM no establece un régimen completo de acceso, sino un supuesto especial de acceso -una prohibición de divulgación de la información facilitada por el laboratorio-. No existe ningún otro artículo en el TRLGURM que establezca normas de acceso a información sobre medicamentos que permita excluir la LTAIBG.
La conclusión obligada es la plena aplicación de las LTAIBG con la sola excepción de la obligación de confidencialidad prevista en el artículo 97.3 TRLGURM.
Segunda. Si la reserva de confidencialidad del artículo 97.3 TRLGURM se limita a la información facilitada por los laboratorios o alcanza también al precio financiado y a las condiciones de financiación.
El artículo 97.3 se refiere única y exclusivamente a la información que facilita la empresa farmacéutica a la Administración sanitaria. Es evidente, por tanto, que la confidencialidad que predica dicho artículo no alcanza ni protege la resolución administrativa que dicta la Administración sanitaria con el precio efectivo y las condiciones de financiación. Y no es viable, como afirma la Audiencia Nacional, que el conocimiento combinado del precio industrial y del precio financiado permitiría inferir datos estratégicos sobre costes, márgenes y condiciones de negociación. Se trata de una afirmación no fundamentada jurídicamente con datos objetivos, esto es, la Audiencia Nacional no explica cómo se hace esa inferencia inversa de manera que resulte creíble. La Audiencia Nacional se limita a acoger acríticamente lo alegado por la farmacéutica demandante que no justifica técnicamente tal inferencia.
Lo que se demanda por las Fundaciones Civio y Salud por Derecho es conocer el precio de un medicamento fijado por la Administración, y las condiciones finales en que se va a financiar, no otros aspectos en base a los cuales se ha determinado el precio, pues en tales aspectos sí se pondrían de manifiesto intereses económicos y comerciales, al guardar directa relación con la posición de competitividad de la empresa o con sus procesos de producción. En suma, no es aceptable que el precio de financiación pública sirva para hacer esas inferencias pues, entre otras muchas razones, el precio del mismo medicamento es diferente según países, según Comunidades Autónomas e, incluso, según hospitales de la misma Comunidad Autónoma.
No es correcta ni posible, pues, una interpretación extensiva del artículo 97.3 que acoja también el precio de financiación pública.
Tercera. Si la garantía de confidencialidad está justificada cuando el proceso de decisión está en curso, o si se extiende también una vez tomada la decisión.
Evidentemente, la información entregada por la empresa farmacéutica a la Administración sanitaria debe seguir siendo confidencial una vez que el proceso de decisión ha concluido y se ha fijado el precio del medicamento.
¿Es extensible esta afirmación al precio fijado por la Administración sanitaria una vez concluido el proceso de decisión? El TRLGURM nada dice al respecto, pero sí la legislación de transparencia pues prevé como límite al acceso a información pública la garantía de la confidencialidad requerida en procesos administrativos de toma de decisión. Y la doctrina elaborada al respecto es muy clara: el límite es aplicable cuando se está en fase de tomar una decisión administrativa importante y su conocimiento público haría variar esa decisión o influir en ella de manera notoria y determinante, tanto en el transcurso de un procedimiento abierto como en situaciones futuras parecidas. Se trata de proteger estos procedimientos de un exceso de transparencia que pudiera perturbarlos. Lo que se busca es que las autoridades llamadas a decidir lo hagan sin la “presión” de un escrutinio público paralelo con todos los elementos de juicio. Por el contrario, si se trata de información sobre expedientes que no se hallan en curso, esto es, sobre los que ya se ha decidido y cuyo conocimiento no condiciona la efectividad de expedientes futuros en la misma materia, este límite no es aplicable. Las recientes sentencias del TS 301/2026, de 11 de marzo de 2026 y 1164/2026, de 11 de marzo de 2026, son claras al respecto al recoger esta doctrina.
Por tanto, en nuestro caso, la garantía de confidencialidad del artículo 97.3 no es aplicable respecto de la decisión tomada pues el proceso de decisión ya ha concluido y conocer el precio de financiación de un medicamento en nada condiciona futuros procesos de decisión para la fijación del precio de otros medicamentos.
III. Sobre la enmienda en el proyecto de ley de discapacidad
Actualmente, se está tramitando en las Cortes Generales el proyecto de Ley sobre derechos de las personas con discapacidad y dependencia. Los grupos parlamentarios Socialista y SUMAR han presentado una enmienda al proyecto, la núm. 259 [III], que propone una nueva disposición final a incorporar en el citado proyecto de Ley, que modificaría el artículo 97.3 del TRLGURM. La enmienda propone sustituir el vigente texto del apartado 3 por el siguiente texto: “Los acuerdos de financiación que se alcancen, así como la información derivada de los mismos o de su aplicación, incluyendo los precios de adjudicación de los contratos de suministro de medicamentos que celebren las Administraciones Públicas, tendrán carácter confidencial”. La enmienda se justifica en lo siguiente: “El riesgo de que una interpretación judicial restrictiva del artículo 97.3 de la Ley de garantías obligue a divulgar precios efectivos y acuerdos de financiación, con efectos estructurales sobre el gasto y el mercado farmacéutico”.
En mi opinión, desde la perspectiva de la ética política es inadmisible que cuando el TS va a sentar doctrina jurisprudencial sobre la opacidad o transparencia de los precios de financiación pública de los medicamentos, doctrina que resolverá definitivamente esta polémica cuestión y a la que deberán atenerse todas las instituciones y entidades, se intente neutralizar ese pronunciamiento jurisprudencial por la torticera vía por la que se está haciendo y, además, sorprende que la enmienda la promuevan dos grupos parlamentarios “progresistas” que se supone son defensores de la sanidad pública, de la transparencia de las decisiones públicas, y de la fijación de precios justos y asequibles basados en los costes reales, con márgenes de beneficios normales, preciso que permitan el acceso universal a los medicamentos.
Como bien dice la Fundación Civio [IV], “la enmienda propone resolver las tres cuestiones de interés casacional por vía legislativa antes de que el TS pueda pronunciarse. La enmienda es un intento de vaciar de contenido un procedimiento judicial en curso, modificando la norma que el TS ha de interpretar, neutralizando, esto es, haciendo inútil la interpretación que haga. Y se hace, además, por la vía más opaca posible: insertando la reforma en una ley de discapacidad, fuera del debate de la Comisión de Sanidad.”
La enmienda recoge fielmente la posición al respecto de Novartis y de la industria farmacéutica en general. Las empresas farmacéuticas sostienen que las decisiones en materia de precios de las autoridades nacionales están interconectadas entre sí, de manera que los países de la UE utilizarían los precios financiados de otros Estados miembros, cuando se hacen públicos, para conseguir reducciones de precios en sus propios sistemas públicos, por lo que las empresas farmacéuticas solo se avienen a negociar reducciones de precios cuando el precio de intervención se mantiene confidencial. Así, un argumento recurrente de la industria farmacéutica es que si no hay confidencialidad los precios del medicamento tenderían a igualarse a un valor único que sería relativamente bajo para los países ricos, pero demasiado alto para los más pobres, complicando un acceso justo por los pacientes. Y que esta dinámica también sucedería en las negociaciones con los Servicios de Salud de las diecisiete Comunidades Autónomas, lo que ocasionaría un perjuicio a nuestro Sistema Nacional de Salud.
Evidentemente, estamos ante un argumento falaz. Las empresas farmacéuticas no son ONGs que, en vez de perseguir el máximo beneficio empresarial, prefieren asegurar el acceso al medicamento por los ciudadanos en los países o regiones pobres, y que para alcanzar ese encomiable objetivo requieren de la confidencialidad del precio que pactan con el comprador. Realmente, son argumentos engañosos. La industria farmacéutica, que son sociedades anónimas mercantiles bastantes de ellas dominadas por fondos de inversión especulativos, persigue exclusivamente hacer negocio. La confidencialidad les es necesaria para poder negociar libremente y obtener el mayor precio posible, para lo que les interesa que un comprador no sepa lo que otro comprador paga por el medicamento. En el año 2015, la Comisión Europea hizo público un documento titulado “Study on enhanded cross-country coordination in the área of pharmaceutical pricing” en el que se concluía que la confidencialidad sobre los precios de los medicamentos no los abarata, y que, si los Estados miembros de la UE compartieran esta información, el coste de los fármacos financiados podría descender significativamente. Por su parte, la OMS aprobó el 28 de mayo de 2019 la Resolución WHA72.8, en la que se afirma que la transparencia de precios no debilita la posición negociadora de los Estados: la refuerza, porque reduce la asimetría informativa entre la administración pública y la industria. La opacidad no protege al Estado; protege a quien tiene más información, que son las empresas farmacéuticas, que conocen los precios que cobran en todos los países.
Ha de resaltarse que la enmienda también predica el secreto sobre los precios de adjudicación de los contratos de suministro de medicamentos, lo que es frontalmente opuesto a la Ley 9/2017, de Contratos del Sector Público (LCSP), que sienta la transparencia como sello distintivo de los procesos de contratación pública (art. 1.3), obligando a publicar los documentos de los contratos, incluido el importe de adjudicación (art. 63.3.b). Cierto que su artículo 154.7 permite que, excepcionalmente, alguna información sea secreta cuando la publicidad pudiera perjudicar determinados bienes jurídicos que inventaria, entre los que enumera intereses comerciales legítimos de empresas públicas o privadas o la competencia leal entre ellas. Ahora bien, en gran parte de la compra hospitalaria de medicamentos los contratos son adjudicados a los laboratorios por procedimientos no concurrenciales -negociado sin publicidad- y en estos casos no es aplicable la excepción del citado artículo 154.7, pues no hay perjuicio a la competencia leal entre empresas -no hay competencia-, y respecto de los intereses comerciales legítimos hasta ahora ninguna farmacéutica adjudicataria de un contrato público ha aportado argumentos mínimamente motivados sobre el perjuicio económico que podría producirle la publicidad del precio del contrato.
IV. Sobre la necesaria transparencia en la gestión de los medicamentos
Un elemento determinante de esta política protectora de la confidencialidad son las patentes de los medicamentos y, particularmente, el abuso que hacen de ellas las farmacéuticas. Durante el periodo de vigencia de las patentes -hasta 20 años-, el laboratorio goza del derecho exclusivo de fabricar el producto, comercializarlo, licenciarlo, importarlo y exportarlo, lo que permite que, en ejercicio de su monopolio, consigan imponer unos precios desmesuradamente altos e impida que se produzcan genéricos a precios asequibles para cualquier economía. Además, las patentes se pueden ampliar cinco años más mediante los Certificados de Protección Suplementaria. Es también frecuente la ampliación de patentes, llamadas patentes secundarias, por innovaciones técnicas (nuevas formulaciones, dosis, usos, etc.) del medicamento patentado[V].
Sin embargo, tradicionalmente los medicamentos se consideraban un bien común que no podía ser objeto de patente. Merece la pena resaltar que Jonas Salk, descubridor de la vacuna contra la polio, enfermedad que mataba o dejaba paralíticas a las personas, en 1953 se negó a patentarla aduciendo que era de la gente, como el sol, un bien público [VI]. Nos relata Martínez Segura[VII] que, en los EE.UU., las patentes de medicamentos se introdujeron en la primera mitad del siglo XX, por la presión de la industria farmacéutica, que quería aumentar sus precios y sus ganancias, y con el rechazo de muchos médicos y sociedades científicas. En Europa, en cambio, se incorporaron más tarde, en 1967 en Alemania, en 1977 en Suiza, o en 1980 en Italia. En España, la Ley de la Propiedad Industrial de 1929, en su artículo 48.2., prohibía las patentes de medicamentos; sin embargo, como consecuencia de nuestra incorporación a la Unión Europea, en 1986 se modificó la Ley de Patentes incluyendo los medicamentos.
La sociedad civil y algunos países (India, Sudáfrica) mantienen una lucha constante por la eliminación o la suspensión temporal de las patentes de medicamentos, pero hasta ahora han fracasado frente a la fuerza del poderoso lobby farmacéutico. Hoy por hoy la eliminación de las patentes de los medicamentos parece totalmente inviable. No obstante, en las leyes reguladoras de las patentes se prevé las llamadas licencias obligatorias como un límite o excepción al derecho de propiedad de la patente, que suspende temporalmente el derecho de exclusividad, de manera que permite la producción, uso, venta o importación por un tercero, sin necesidad de consentimiento alguno, mediante un canon o remuneración adecuados [VIII]. Es legítimo hacer uso de la licencia obligatoria por razones de interés público -protección de la salud pública-. Sin embargo, en nuestro país nunca se ha utilizado este instrumento.
Actualmente, los medicamentos innovadores patentados y autorizados que salen al mercado tienen unos precios excesivamente altos, que en absoluto se corresponden con el costo real de los mismos. De ahí que el gasto farmacéutico público se haya disparado hasta el punto de que está poniendo en cuestión la sostenibilidad del sistema sanitario público. Según un estudio [IX] resulta que, de los 25.000 millones de euros de gasto farmacéutico público de 2024, más de 10.000 millones de euros son gasto innecesario, injusto, en precios abusivos de los medicamentos. Ello trae causa de que los fondos de inversión que controlan las empresas farmacéuticas están utilizando el secretismo que rodea el costo de la investigación biomédica, que en buena parte es financiada directa o indirectamente con dinero público, y los monopolios que permiten las patentes de los medicamentos, como un instrumento especulativo para generar enormes beneficios privados.
Aplicando el test del interés público a las solicitudes de acceso a decisiones administrativas sobre medicamentos de financiación pública, un producto que afecta muy directamente a la vida y la salud de las personas, no cabe duda de que siempre ha de prevalecer el interés público sobre el interés comercial de las empresas farmacéuticas, toda vez que el medicamento es un bien público de primera necesidad absolutamente necesario para hacer efectivo en lo posible al derecho humano a la protección de la salud. No es una mera mercancía que pueda ser objeto de especulación. Es un bien que por sus características intrínsecas -curar, prevenir o aliviar las enfermedades- tiene un interés superior al que pueda resultar de su consideración como un bien susceptible de comercio. Es un elemento esencial del sistema sanitario de cualquier país. Entonces, a efectos de garantizar el acceso universal al medicamento, existe claramente un interés público superior en conocer cómo se toman las decisiones en las políticas públicas de financiación del medicamento y cómo se gasta el dinero público dedicado a la prestación farmacéutica. Y este interés público siempre ha de prevalecer sobre el interés privado mercantil de una empresa farmacéutica pues el conocimiento por la sociedad de las decisiones administrativas en torno al medicamento le permitirá participar activa y responsablemente en un sistema sanitario que garantiza un derecho humano fundamental cual es la vida y la salud de las personas.
Se argumenta por las empresas farmacéuticas que si no se mantuviera confidencial el precio de venta de laboratorio y el descuento ofertado por el laboratorio, su publicidad resultaría contraria a los intereses de la Administración sanitaria de España, en tanto que perjudicaría a la obtención de ahorros en el gasto farmacéutico y, por tanto, un perjuicio grave a nuestro sistema sanitario, máxime en el caso de medicamentos que se producen en exclusividad y que no cuenta con alternativa en el mercado. De ahí que el interés público de la Administración sanitaria, consistente en el acceso a la adquisición del medicamento y en el beneficio de contar con el referido descuento comercial en el precio de las dosis adquiridas, justificarían la procedencia de la confidencialidad señalada por la empresa en cuanto a los términos de su oferta[X].
Sin embargo, cuando se contrata con el sector público, se debe saber que la estrategia comercial no se puede imponer a las obligaciones de transparencia que la legislación de transparencia impone a las entidades públicas y que exigen que se difundan, en régimen de publicidad activa, los elementos esenciales de los contratos formalizados por el sector público, y su precio en concreto, en atención al interés general existente en la aplicación del marco legal de publicidad y transparencia en la contratación pública, establecido como mecanismo de prevención de la corrupción, así como el interés público prevalente en la garantía de la rendición de cuentas y de la responsabilidad en la gestión pública. En suma, en el caso del medicamento concurre un interés público superior en la publicación de esa información toda vez que es un bien público de primera necesidad absolutamente imprescindible para hacer efectivo en lo posible el derecho humano a la protección de la salud. No es una mera mercancía que pueda ser objeto de especulación. Es un bien que por sus características intrínsecas -curar, prevenir o aliviar las enfermedades- tiene un interés superior al que pueda resultar de su consideración como un bien susceptible de comercio.
En el actual sistema de total opacidad no existe rendición de cuentas del gasto de dinero público en la financiación de medicamentos, lo que desnaturaliza, cuando no imposibilita, el debate público documentado y riguroso sobre las políticas de financiación de los medicamentos, hurtando a la sociedad una exigible rendición de cuentas, y el conocimiento necesario para poder valorar, proponer y exigir medidas que garanticen el acceso universal al medicamento. Y esta indeseable situación está violando el derecho humano a la protección de la salud, derecho que incluye la atención sanitaria y el acceso a los medicamentos necesarios. Las decisiones de la Administración sanitaria en lo que hace a la incorporación o no a la cartera de prestaciones y a la financiación pública de los fármacos afecta muy directamente a la vida de las personas.
Referencias
[I] Entre otras, R 231/2017; R239/2018; R266/2018; R79/2019; R885/2019; R47/2020; R 522/2021; R 1076/2021; R 123/2022; 52/2023; R 204/2023;
[II] Por un cambio de la normativa procesal, este procedimiento ordinario no se reside, como los otros casos, en el Juzgado Central, sino directamente ante la Audiencia Nacional -Sección Séptima-.
[III] BOCG. Congreso de los Diputados, serie A, núm. 64-5, de 12 de marzo de 2026.
[IV] Carta dirigida por la Fundación Ciudadana Civio a los miembros de la Comisión de Derechos Sociales y Consumo del Congreso de los Diputados, file:///C:/Users/piluc/OneDrive/Downloads/Carta%20Comisio%CC%81n%20Derechos%20Sociales_Enmienda%20259%20al%20PL%20121_000064.pdf
[V] En relación con las patentes secundarias, la STS 625/2025, 24 de abril de 2025, consolida en España la doctrina de la Oficina Europea de Patentes de la «plausibilidad del efecto técnico” para la actividad inventiva, según la cual no basta con una mera afirmación del efecto técnico: es necesario que el efecto resulte verosímil o razonablemente sustentado. En definitiva, la invención debe presentar una base técnica suficiente en la fecha de presentación que haga verosímil el efecto técnico alegado, evitando patentes meramente especulativas.
[VI] Véase 29 años sin Jonas Salk: contra la normalización del absurdo en Revista AAJM, nº 31, junio de 2024, pp. 27-28.
[VII] Véase ¿Son los medicamentos “res communis”? en Revista AAJM, nº 23, septiembre de 2023, p.3-7.
[VIII] Sobre licencias obligatorias y su reciente normativa, véase Francisco Javier Carrión García de Parada y Francisco López Blanco, “Licencias obligatorias de patentes y otros derechos de propiedad industrial. El nuevo reglamento (UE) de 16 de diciembre de 2025 sobre la concesión de licencias obligatorias para la gestión de crisis y por el que se modifica el Reglamento (CE) nº 816/2006”, Cuadernos de Derecho Farmacéutico, nº 96, 2026, pp. 36-51
[IX] Publicado en el número 35 de la revista AAJM, de enero de 2025, titulado Análisis del documento “Estrategia de la Industria Farmacéutica 2024-2028”, del Gobierno de España, pp. 22-30.
[X] Una recopilación de los artículos y estudios publicados en favor de la opacidad de los precios de medicamentos de financiación pública puede verse en el número especial monográfico de Cuadernos de Derecho Farmacéutico publicado en 2025.
OTRAS FUENTES. Revista nº47 de Abril de 2026

Public Citizen.
Public Citizen, 30-04-2026. https://www.citizen.org/news/u-s-trade-report-boosts-big-pharma-and-attacks-health-safeguards/
El día 30 de abril, Public Citizen publicó una noticia donde expone una decisión de EE.UU de singular importancia para la Unión Europea. El Informe Especial 301 ha incluido este año a la Unión Europea en su “Lista de Vigilancia”. La sección 301 es una herramienta ampliamente utilizada por Estados Unidos, para amenazar con sanciones y disciplinar a aquellos países que considera amenazan a sus empresas y a sus intereses en la política comercial. Efectivamente aquellas naciones que mediante la utilización de regulaciones nacionales propias intentan mejorar el acceso de sus ciudadanos a los medicamentos necesarios para recuperación de la salud son amenazadas inmediatamente con la aplicación de sanciones económicas.
Peter Maybarduk, director de Acceso a Medicamentos de Public Citizen, afirma que la lista 301 de este año es más lesiva pues va más allá de las políticas habituales sobre patentes y comercio para atacar directamente las regulaciones nacionales sobre accesibilidad.
Sin duda, esta forma de presión sobre la UE es un elemento más añadido, a las acciones del gobierno Trump, durante los tres últimos meses, con la amenaza de utilización de imposición, de aranceles abusivos a los países de Europa. (como hemos visto recientemente con Reino Unido y Francia).
Posiblemente, una actitud más valiente y decidida de la Unión Europea, y en nuestro caso de España, dirigida a fortalecer las regulaciones propias que garanticen de forma real y efectiva un acceso justo en los medicamentos, sería sin duda un elemento positivo de resistencia frente a abuso y la imposición.
(Sin embargo, estimados lectores, esta posibilidad parece muy lejana en el escenario actual, cuando observamos, por ejemplo, en nuestro ámbito español, como el secretario de Estado decide contentar a la industria farmacéutica con la decisión asombrosa de blindar la falta de transparencia sobre la negociación de los precios de los medicamentos).
WASHINGTON, D.C. — Hoy, la Oficina del Representante Comercial de Estados Unidos publicó su anual Informe Especial 301, que señala a socios comerciales por supuestamente no brindar protecciones de propiedad intelectual o acceso al mercado “adecuados”. Public Citizen presentó comentarios en el proceso anual de revisión del Informe Especial 301, que sirve de base para el citado informe.
En su respuesta, expertos de Public Citizen afirmaron que el informe fomenta la explotación corporativa de la política comercial y ataca regulaciones, incluidas las de la Unión Europea (que se agregó a la “Lista de Vigilancia” del informe este año) y de otros países que contribuyen a reducir los precios de los medicamentos, las cuales se están considerando activamente en Estados Unidos, socavando así nuestros esfuerzos nacionales para salvaguardar la salud y responder a los abusos de poder corporativos:
“Al agregar a Europa a su lista de vigilancia, los representantes comerciales de Trump demuestran que servirán a las grandes farmacéuticas y aumentarán los precios de los medicamentos, incluso si tienen que retorcer la lógica como un pretzel bávaro”, declaró Peter Maybarduk, director de Acceso a Medicamentos de Public Citizen.
Esta lista 301 profundiza más y de forma más invasiva que en años anteriores, atacando políticas nacionales de asequibilidad que nada tienen que ver con patentes o comercio.
“La medicina asequible es algo positivo. El pueblo estadounidense así lo cree. Podríamos aprender de estos países.” se afirma Sin embargo Trump está usando todo su poder para atacar a los socios comerciales de EE. UU. que están haciendo que la medicina sea más asequible. Todos pierden, excepto la BigPharma, la gran industria farmacéutica.
“Los recientes Acuerdos de Comercio Recíproco (ART) de Trump llevan el acoso en nombre de la industria farmacéutica a nuevos niveles mediante medidas vinculantes que exigen cambios en las leyes de los socios comerciales basándose directamente en la lista negra especial 301 de los fabricantes de medicamentos de marca”, declaró Melinda St. Louis, directora de Public Citizen Global Trade Watch. “Por ejemplo, la administración Trump celebra su éxito al utilizar aranceles ilegales para lograr que Argentina cambie sus leyes sanitarias. El informe deja claro que la política comercial de Trump no busca proteger los empleos estadounidenses, sino atacar las políticas de interés público, tanto nacionales como internacionales, en beneficio de los magnates farmacéuticos y otros amigos multimillonarios”
OTRAS FUENTES. Revista nº47 de Abril de 2026
The Bureau of Investigative Journalism.
Global Health, 13-04-2026. https://www.thebureauinvestigates.com/stories/2026-04-13/inside-the-64bn-pharma-deal-that-could-cost-more-lives-than-covid
Este artículo ilustra muy bien cómo se ha realizado el acuerdo farmacéutico entre el Reino Unido y los Estados Unidos. Un acuerdo que realmente no puede denominarse como tal, pues en realidad se ha producido por la imposición de Estados Unidos con la complicidad activa de las compañías farmacéuticas en un proceso “negociador” marcado por los lobbies y la corrupción política
Las consecuencias en la salud de la población atendida por el NHS por la decisión de pagar más a las compañías farmacéuticas, se traducirá en miles de vidas perdidas.
Un vistazo previo
Todo comenzó con un mensaje de texto enviado a principios de 2025
“Se avecina un gran problema con los aranceles a la industria farmacéutica”. Fue uno de los muchos mensajes intercambiados entre Peter Mandelson, entonces embajador del Reino Unido en Estados Unidos, y el secretario de Salud, Wes Streeting.
“Trump cree que la industria farmacéutica estadounidense no recibe un trato justo, quiere imponer aranceles a la UE y al Reino Unido y obligar a la producción a trasladarse a Estados Unidos”, advirtió Mandelson.
Un vistazo previo
El nuevo acuerdo farmacéutico entre el Reino Unido y los Estados Unidos significará que el NHS pagará más a las compañías farmacéuticas por sus medicamentos
Se prevén cientos de miles de muertes durante 10 años debido a que el dinero se desvía de actividades de atención médica
Las afirmaciones del gobierno sobre el valor del acuerdo se ven eclipsadas por los cálculos de los expertos sobre su verdadero costo
Todo comenzó con un mensaje de texto enviado a principios de 2025.
“Se avecina un gran problema con los aranceles a la industria farmacéutica”.
Fue uno de los muchos mensajes intercambiados entre Peter Mandelson, entonces embajador del Reino Unido en Estados Unidos, y el secretario de Salud, Wes Streeting.
“Trump cree que la industria farmacéutica estadounidense no recibe un trato justo, quiere imponer aranceles a la UE y al Reino Unido y obligar a la producción a trasladarse a Estados Unidos”, advirtió Mandelson.
La respuesta de Streeting fue concisa: “¡Uf!”.
El año siguiente estuvo marcado por largas negociaciones entre funcionarios estadounidenses y británicos encargados de alcanzar un acuerdo comercial entre ambos países. Se produjo un enfrentamiento de meses entre el Reino Unido y la industria farmacéutica. Y finalmente, se llegó a un controvertido acuerdo entre ambos países que, desde entonces, ha permanecido envuelto en el secretismo.
Fuera del acuerdo, el sistema de salud británico sobrevive a duras penas bajo una enorme presión. Datos del Real Colegio de Medicina de Urgencias muestran que, en 2024, alrededor de 320 pacientes fallecieron semanalmente en Inglaterra debido a retrasos en la atención de urgencias, l que podrían haberse evitado. En todo el país, más de 7 millones de personas permanecieron en listas de espera del NHS (Servicio Nacional de Salud).
Las negociaciones entre el Reino Unido y Estados Unidos estuvieron marcadas por diversas amenazas hacia el Reino Unido. La administración Trump planteó la posibilidad de aranceles perjudiciales. Las compañías farmacéuticas, cuyos márgenes de beneficio estaban en juego, amenazaron con cancelar importantes proyectos en el Reino Unido.
Cuando finalmente se alcanzó un acuerdo, el gobierno británico declaró que este costaría al NHS en Inglaterra mil millones de libras esterlinas en los próximos tres años. Los expertos afirman que esta cifra representa solo una fracción del coste real.
En cuanto al acuerdo en sí, obliga al NHS a gastar más en medicamentos nuevos y costosos, así como a pagar más por los fármacos que ya adquiere.
También afecta la forma en que el NICE, el organismo que decide qué medicamentos puede comprar el NHS en Inglaterra y Gales (Escocia e Irlanda del Norte también se benefician de estas decisiones), evaluará los nuevos fármacos. Este cambio en el umbral del NICE implica que probablemente se aprueben algunos medicamentos que antes se habrían rechazado por motivos de rentabilidad, lo que supone, una vez más, una reducción del presupuesto del NHS.
El NICE declaró: «Nuestras decisiones buscan un equilibrio entre poner tratamientos innovadores a disposición de los pacientes y garantizar el mejor uso de los fondos públicos».
Acuerdos como este entre Estados Unidos y el Reino Unido son vitales para que los pacientes británicos reciban medicamentos que salvan vidas. Sin embargo, los críticos del acuerdo afirman que desviar fondos de las salas de hospital, los servicios de urgencias y otras formas de atención vitales costará vidas. En una carta abierta a Streeting, más de 200 expertos, activistas y profesionales sanitarios calificaron el acuerdo de «catástrofe» para todos los pacientes del NHS. En ella describen las posibles consecuencias como «trágicas» e «impactantes».
Karl Claxton, destacado economista de la salud que formó parte del comité de evaluación del NICE, dirigió un equipo de investigadores de la Universidad de York para modelar los posibles resultados. Sus conclusiones son contundentes: «Para 2033, el exceso de muertes derivado de este acuerdo será mayor que el causado por la COVID-19».
Más letal que la COVID-19.
Investigadores de la Universidad de York proyectan que el acuerdo farmacéutico del Reino Unido provocará más muertes adicionales que las sufridas durante dos años de pandemia.
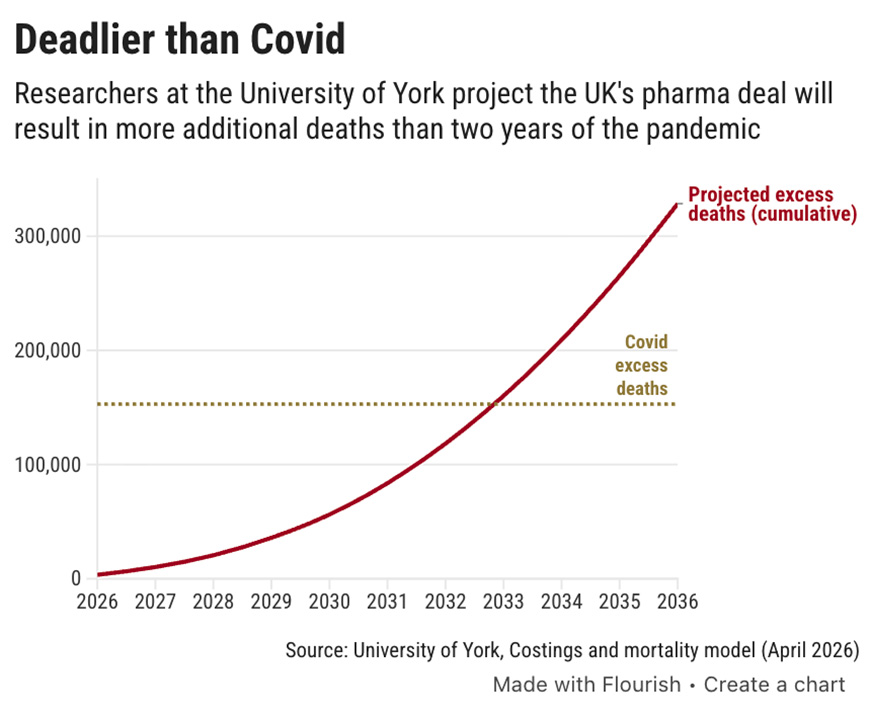
La versión oficial es diferente. Un portavoz del gobierno cuestionó los cálculos. El acuerdo, afirmó, «es una inversión vital que se basa en la solidez de nuestro Servicio Nacional de Salud (NHS) y en el sector de las ciencias de la vida, líder a nivel mundial, para aumentar el acceso a medicamentos que salvan vidas sin desviar fondos esenciales de nuestros servicios sanitarios de primera línea».
La Asociación de la Industria Farmacéutica Británica (ABPI) desestimó la investigación de la Universidad de York por considerarla «fundamentalmente errónea». El NICE declaró estar al tanto de la investigación académica sobre la fijación de precios de los medicamentos, incluyendo el trabajo de York, y que «toma en serio este tipo de análisis».
«El NICE revisa y actualiza continuamente sus métodos para garantizar que sigan representando las mejores prácticas en la evaluación de tecnologías sanitarias», añadió.
Pero a pesar de las enormes implicaciones del acuerdo para la salud pública, al Parlamento no se le ha permitido revisar sus términos. A activistas y periodistas se les han denegado solicitudes de acceso a la información para obtener detalles clave. Las preguntas de los políticos no han recibido respuestas satisfactorias.
Entonces, ¿cómo ha podido el gobierno llegar a un acuerdo que elude el escrutinio democrático? ¿Y cuáles fueron sus razones para aceptarlo?
Dentro de las negociaciones
En las semanas posteriores al mensaje de texto de Mandelson a Streeting, las fuerzas que moldearían las negociaciones, tanto nacionales como internacionales, se hicieron rápidamente evidentes.
El primer punto de controversia fue el programa de reembolso de medicamentos del Reino Unido, que, en marzo del año pasado, la ABPI afirmó que estaba haciendo que el país fuera «poco atractivo para la inversión». Según este programa, el NHS acepta un límite de gasto determinado en medicamentos de marca y obliga a las compañías farmacéuticas a devolver cualquier gasto excesivo. (Según la ABPI, las compañías farmacéuticas devolverían 13.500 millones de libras esterlinas en cuatro años con la normativa actual).
El verano pasado, la industria farmacéutica exigió un aumento de precios de alrededor de 2.500 millones de libras esterlinas anuales a través del programa. Los ministros lo rechazaron y propusieron inyectar 1.000 millones de libras esterlinas en el mercado durante tres años. La industria farmacéutica se negó. Streeting afirmó que no permitirá que las compañías farmacéuticas se aprovechen de los pacientes.
Lobby (cabildeo) a larga distancia
PhRMA, el grupo de presión en Washington que representa a las grandes farmacéuticas estadounidenses, lleva años presionando al NICE y al sistema de precios de medicamentos del Reino Unido.
Lo que diferenció las negociaciones del año pasado fue «la agresividad con la que Trump está dispuesto a oponerse a estos controles de precios», afirmó Nick Dearden, de Global Justice Now.
Resulta sorprendente cómo ciertos elementos del acuerdo —el aumento del umbral del NICE y el límite del 15 % en el programa de descuentos— coinciden casi a la perfección con las antiguas demandas de PhRMA.
También surgen dudas sobre quién influyó en la postura negociadora del Reino Unido. Peter Mandelson, embajador del Reino Unido en Washington durante la fase clave de las negociaciones, es también cofundador de la consultora Global Counsel. Según los registros oficiales, esta consultora ejerció presión en nombre de importantes empresas estadounidenses, como GSK, hasta el verano de 2024.
Durante las negociaciones, la ABPI encargó a Global Counsel un estudio que justificaba muchos de los cambios finalmente alcanzados en el acuerdo. ABPI afirmó que Global Council facilitó talleres durante la elaboración del informe, el cual se produjo bajo su control exclusivo, y añadió que colabora con diversas organizaciones para la producción de sus publicaciones.
El Ministerio de Asuntos Exteriores rechazó nuestra solicitud de información sobre las reuniones de Mandelson con compañías farmacéuticas, alegando que obtener dicha información resultaría demasiado costoso. PhRMA no respondió a las solicitudes de comentarios.
Al otro lado del Atlántico, Donald Trump intentaba obligar a las farmacéuticas a bajar los precios de los medicamentos recetados en EE. UU. a los niveles de otros países ricos. En cartas enviadas a 17 empresas en julio, expresó su deseo de poner fin al aprovechamiento indebido de la innovación estadounidense por parte de las naciones europeas y otras desarrolladas. Ya había afirmado que los pacientes estadounidenses «subsidian» el desarrollo mundial de medicamentos.
(Investigaciones realizadas por economistas de la salud demuestran que Trump está equivocado. Con los precios actuales de los nuevos medicamentos, el Reino Unido ya paga lo que le corresponde, lo que significa que las farmacéuticas pueden cubrir el costo de la investigación y el desarrollo de fármacos y aun así obtener ganancias).
En julio del año pasado, el embajador de EE. UU. en el Reino Unido, Warren Stephens, se reunió con ejecutivos de farmacéuticas estadounidenses en Londres para analizar lo que denominó los «retos y oportunidades de operar en el Reino Unido».
Luego, en el transcurso de una sola semana en septiembre, se desencadenó una reacción en cadena. Una tras otra, las empresas amenazaron con retirar importantes proyectos en el Reino Unido: MSD canceló un centro de investigación en Londres valorado en mil millones de libras; AstraZeneca suspendió un proyecto de 200 millones de libras en Cambridge; Eli Lilly aplazó la construcción de un laboratorio previsto en Londres. Ante la preocupación de que los gigantes farmacéuticos hubieran conspirado para aumentar los precios de los medicamentos, la Autoridad de Competencia y Mercados declaró que había decidido no investigar.
A finales de septiembre, los directores ejecutivos de las farmacéuticas comparecieron ante una comisión de la Cámara de los Comunes para responder preguntas sobre la suspensión de sus inversiones en el Reino Unido. Su mensaje fue claro: el NHS (Servicio Nacional de Salud) debía pagar más por sus medicamentos.
Patrick Vallance, ministro de Ciencia del Departamento de Ciencia, Innovación y Tecnología (DSIT) y antiguo jefe de I+D de GSK, supervisaba las negociaciones. En octubre, confirmó que el gobierno británico estaba dispuesto a que el NHS aumentara su gasto en medicamentos de marca.
Aun así, Estados Unidos se mantuvo firme: un mes después, Stephens insistió en que las farmacéuticas estadounidenses cerrarían sus plantas en el Reino Unido si el NHS no aumentaba su presupuesto.
En diciembre, el acuerdo se cerró.
La interpretación de Claxton sobre la situación es sencilla: «El gobierno se enfrentó a una clara disyuntiva», afirmó, «o apoyaba al NHS y a la atención social para adultos y resistía estas presiones, o no. Y decidió no hacerlo».
Los costes reales
Los ministros han presentado el acuerdo como una victoria: cero aranceles estadounidenses a los productos farmacéuticos británicos, crecimiento económico, inversión y empleos que «refuerzan la posición del Reino Unido

Como potencia en ciencias de la vida». La asociación de la industria farmacéutica lo calificó de «buenas noticias para los pacientes del NHS».
Los detalles siguen siendo poco claros. Al preguntarle qué cifra habría aceptado, o aceptaría en las negociaciones la industria farmacéutica, la APBI declaró que «no comenta los detalles de las conversaciones confidenciales de la industria con el gobierno».
El NHS England nos informó de que cuenta con un equipo especializado que negocia acuerdos comerciales confidenciales con las compañías farmacéuticas para garantizar una mejor relación calidad-precio para el público.
Lord Vallance afirma que el acuerdo costará al NHS England mil millones de libras esterlinas en los próximos tres años. E incluso si se aceptara ese coste al pie de la letra, argumenta Claxton, esos mil millones de libras podrían utilizarse mejor. «La mejor manera de gastarlo no es dárselo a la industria farmacéutica», dijo. «La mejor manera de gastarlo es aumentar los presupuestos del NHS o de la atención social para adultos».
Pero afirma que la cifra que dio Vallance debería ser más cercana a los 3.300 millones de libras. Y el coste real del acuerdo para todo el Reino Unido —una vez que se tenga en cuenta el compromiso del gobierno de duplicar el gasto farmacéutico para 2036— será muchísimo mayor: casi 64.000 millones de libras.
Estas cifras tendrán consecuencias drásticas en la práctica. Su equipo predice que otras 330.000 personas podrían morir en el Reino Unido para 2036 como resultado de que el acuerdo desvíe fondos de otras áreas del NHS (Servicio Nacional de Salud), una cifra superior al exceso de muertes registrado durante los dos primeros años de la COVID-19.
En resumen
El gobierno británico ha valorado el acuerdo en 1.000 millones de libras. Los investigadores afirman que el coste real a lo largo de 10 años será muchísimo mayor.
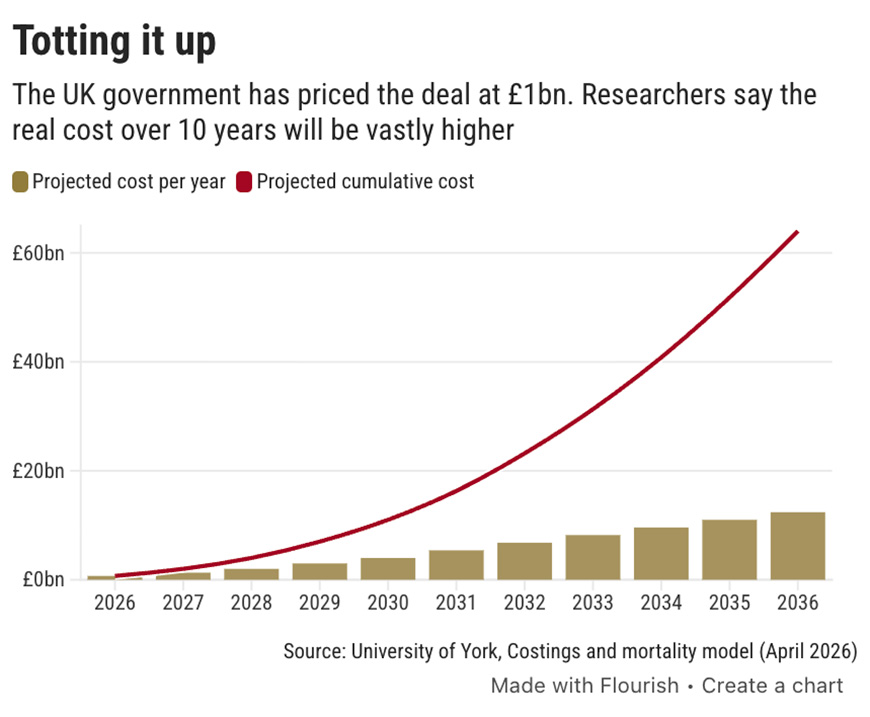
Un portavoz del gobierno nos dijo que las cifras de Claxton “se basan en suposiciones y proyecciones que el gobierno no comparte y no reflejan cómo se toman en la práctica las decisiones sobre la financiación y el acceso a los medicamentos”.
Mathew Hulbert, exconcejal de Leicestershire, no necesita modelos complejos para comprender el coste de un Servicio Nacional de Salud (NHS) con financiación insuficiente. En julio de 2022, su madre de 78 años se cayó y se fracturó las costillas en casa. Mientras yacía en el suelo con dolor, llamó al 999 y le dijeron que no la moviera. “Fueron las 11 peores horas de mi vida”, recuerda. Su madre fue trasladada al hospital, pero falleció dos días después.
Mathew supo más tarde el motivo de la demora: las ambulancias estaban acumuladas a las afueras del Hospital Royal Infirmary de Leicester, sin poder descargar a los pacientes porque las salas ya estaban llenas. “Fue un fallo de todo el sistema”, afirmó.
La historia de Mathew es una de lasmiles que demuestran cómo los recortes en el NHS pueden marcar la diferencia entre la vida y la muerte. Los críticos del acuerdo farmacéutico temen que el dinero adicional destinado a nuevos medicamentos no haga sino agravar la crisis.
Expertos independientes consultados afirmaron que el acuerdo afectará a todos los pacientes del NHS, desde un aumento de la mortalidad y una menor supervivencia relacionadas con el cáncer, las enfermedades respiratorias y gastrointestinales, hasta una disminución de la calidad de vida de las personas con problemas neurológicos, endocrinos y de salud mental.
También se cuestiona si algunos de los nuevos medicamentos que se están adquiriendo a precios elevados representan un mejor uso del dinero que los tratamientos más antiguos y de eficacia comprobada.
Las investigaciones demuestran que varios tratamientos cotidianos del NHS, como las vacunas contra la gripe, los medicamentos para la presión arterial y los ejercicios de rehabilitación para enfermedades pulmonares, brindan atención médica eficaz a una fracción del costo de los medicamentos de marca más recientes.
Secretos y vidas
A pesar de que el acuerdo tendrá un enorme impacto en el gasto del NHS y en el acceso de los pacientes a los medicamentos, el gobierno se ha negado a divulgar detalles clave sobre lo que realmente ha acordado.
Enviamos solicitudes de acceso a la información tanto al Departamento de Salud y Asistencia Social (DHSC) como al Departamento de Tecnología de la Información y la Comunicación (DSIT) solicitando una copia de la evaluación del impacto del acuerdo. Ambos departamentos se negaron a facilitarla.
El DHSC afirmó que divulgar la información podría debilitar la posición negociadora del Reino Unido y perjudicar las futuras relaciones comerciales con el sector farmacéutico. El DSIT, por su parte, confirmó la existencia de un anexo no publicado a la evaluación de impacto, pero indicó que no lo hará público debido a las relaciones internacionales.
«¿No nos permiten verlo porque podría molestar a Donald?», declaró Seamus Logan, miembro del Parlamento por el Partido Nacional Escocés, al enterarse de estas negaciones. «Es indignante. Absolutamente indignante».
«Hasta la fecha, no ha habido ningún escrutinio parlamentario sobre el funcionamiento de este acuerdo, y es absolutamente necesario que lo haya», afirmó. «Necesitamos saber cuál será el coste real de este acuerdo».
Nick Dearden, de la organización sin ánimo de lucro Global Justice Now, declaró: «Cuando se trata de una regulación política interna como el control de precios del NHS, me parece extraordinario que ni el público ni los parlamentarios tengan acceso a los cálculos».
Al preguntar al gobierno escocés sobre el acuerdo, nos comunicó que «no tuvo ninguna participación en el proceso, a pesar del claro impacto en Escocia y en nuestro NHS». Si bien afirmó que el acuerdo también debería impulsar la inversión, también reconoció que el gobierno británico ha hecho concesiones sustanciales.
Desde que se anunció el acuerdo, ha crecido la preocupación entre los diputados laboristas, liberaldemócratas, verdes y del SNP sobre sus detalles y su coste para el NHS.
Los liberaldemócratas han pedido a Keir Starmer que cancele el «impuesto Trump» al NHS e invierta en la mejora de la atención social. «Estamos muy, muy, muy preocupados de que se desvíen fondos de los servicios esenciales, donde ya nos encontramos en una situación de crisis», afirmó la diputada Helen Morgan.
Añadió que le preocupa cualquier tipo de acuerdo con Estados Unidos, ya que Trump no ha cumplido con los acuerdos anteriores. De hecho, aunque el Reino Unido y Estados Unidos han firmado el acuerdo, este no es jurídicamente vinculante ni según la legislación británica ni la internacional. Esto significa que los acuerdos relativos a las exportaciones británicas a Estados Unidos están sujetos a cambios, incluidos los aranceles cero.
Parece que los estadounidenses están satisfechos. El secretario de Salud de Estados Unidos, Robert F. Kennedy, agradeció a Trump por «obtener resultados que priorizan a los estadounidenses», y el secretario de Comercio, Howard Lutnick, afirmó que el acuerdo implicaría que «los avances del futuro se desarrollarán, probarán y producirán en suelo estadounidense».
En cuanto a las farmacéuticas que amenazaron con abandonar el Reino Unido, aún no se han comprometido a quedarse. AstraZeneca y Bristol Myers Squibb no respondieron a nuestras preguntas. La última declaración de Eli Lilly, que había suspendido su proyecto de laboratorio en Londres, fue que la confirmación del acuerdo era alentadora y que la compañía «revisará sus planes de inversión allí a medida que mejore el entorno». En otras palabras: todavía no.
¿Qué sigue?
Una propuesta presentada ante el Parlamento en marzo otorgará a los ministros la facultad de indicar al NICE qué umbral financiero utilizar para decidir si aprueba o no un nuevo medicamento. Este cambio normativo, derivado del nuevo acuerdo entre el Reino Unido y Estados Unidos, implica que algunos medicamentos ahora recibirán luz verde a un precio que antes se consideraba poco rentable.
Los activistas temen que las compañías farmacéuticas puedan ejercer presión sobre los ministros para obligarlos a realizar cambios en el NICE que no redunden en beneficio de la salud pública, afirma Diarmaid McDonald, del grupo de defensa de pacientes JustTreatment.
Los parlamentarios pueden oponerse a estas propuestas. Entendemos que algunos diputados laboristas planean tomar medidas antes del 27 de abril. Grupos como JustTreatment, Global Justice Now y All Eyes On presionarán para lograr una mayor transparencia sobre el impacto en los pacientes de todo el Reino Unido.
OTRAS FUENTES. Revista nº47 de Abril de 2026
Patrick Durisch.
Public Eye. 13-04-2026.https://www.publiceye.ch/en/topics/pharmaceutical-industry/price-of-medicines-walls-of-abusive-patents-are-standing-in-the-way-of-competition/a-dose-of-this-cancer-drug-costs-more-than-an-ounce-of-gold
Excelente texto, que responde a una investigación realizada por Public Eye y el Consorcio Internacional de Periodistas de investigación sobre el fármaco Keytruda de Merck Sharp&Dohme (MSD). Un medicamento que ha conseguido para MSD unos ingresos totales de 162.000 $.
El artículo describe con claridad el precio abusivo del medicamento y las maniobras de MSD a través de las marañas de patentes para prolongar el tiempo de monopolio y por tanto de exclusividad comercial en el mercado. Asimismo, el trabajo refuta con datos, la argumentación habitual de la BigPharma intentando justificar los elevados precios por los costes de la inversión en investigación y los altos riesgos de esta.
Patrick Durisch se dirige a los gobiernos instando a que exijan la divulgación de las Inversiones reales realizadas por las empresas farmacéuticas y a la financiación pública que reciben y por tanto a la necesidad ineludible de reformar el sistema actual unilateral de fijación de precios de los medicamentos. Animamos a nuestras y nuestros lectores a su lectura.
Comercializado desde finales de 2014, Keytruda está autorizado en Estados Unidos, Europa y Suiza para el tratamiento de más de 20 tipos de cáncer, desde cánceres del sistema digestivo y los pulmones hasta cánceres de piel, hígado, sangre, órganos reproductores, riñones y mama.
Sobre todo, ha permitido a la empresa estadounidense Merck Sharp & Dohme (MSD) generar ingresos asombrosos: 31.700 millones de dólares (unos 25.000 millones de francos suizos) en 2025, solo con este producto, una cifra casi equivalente al producto interior bruto (PIB) de Senegal o Islandia. Tras 11 años en el mercado, Keytruda ha generado para MSD unas ventas totales de 162.800 millones de dólares, lo que impulsó al grupo al cuarto puesto en el ranking de las grandes farmacéuticas en 2025.
Al igual que Herceptin o Perjeta de Roche (véase nuestro episodio de noviembre de 2025), Keytruda es un fármaco biológico compuesto por anticuerpos monoclonales. Pertenece a la categoría de inmunoterapias: tratamientos que estimulan el sistema inmunitario para atacar las células cancerosas. Estos fármacos han transformado indudablemente la atención oncológica, permitiendo controlar la enfermedad y prolongar la vida de muchos pacientes. Sin embargo, este tratamiento «milagroso» tiene un precio exorbitante, lo que conlleva restricciones de acceso y un aumento vertiginoso de los costes sanitarios, como detallamos en nuestra investigación. Public Eye compartió sus análisis con el Consorcio Internacional de Periodistas de Investigación (ICIJ) y sus socios de medios.
Precios prohibitivos en Suiza y en el extranjero
Keytruda se vende a un precio elevado en todos los países donde se comercializa. En Suiza y la Unión Europea (UE), el precio real (neto) del medicamento, negociado entre MSD y los gobiernos, es confidencial (véase más abajo). No obstante, el precio de lista de Keytruda —a veces denominado precio de referencia— da una idea de las sumas involucradas. Y las cifras son vertiginosas.
En Suiza, Keytruda encabeza la lista de los medicamentos más costosos elaborada por la aseguradora de salud Helsana, que estima su coste oficial en 183,4 millones de francos suizos para 2024 (las cifras para 2025 aún no están disponibles). El precio oficial del medicamento —cubierto por el seguro médico obligatorio desde 2015— es de 4294 francos suizos por un envase de 200 mg (dosis estándar), lo que equivale a más del precio de una onza de oro. Según nuestros cálculos, esto supone un coste de 73.000 francos suizos por persona para un tratamiento anual, y más de 160.000 francos suizos si se incluyen otros tratamientos con los que se puede combinar.
El precio de lista (o precio de referencia) es un precio público y ficticio para un medicamento. Difiere del precio real cubierto por el sistema sanitario, que suele ser confidencial y se negocia entre la farmacéutica y cada gobierno.
En Suiza, la Oficina Federal de Salud Pública (OFSP), responsable de fijar los precios de los medicamentos, utiliza cada vez más los denominados «modelos de precios» (o acuerdos de acceso gestionado) para cumplir con los requisitos de rentabilidad de la ley de seguro médico obligatorio (LAMal). En la práctica, la OFSP y la farmacéutica llegan a un acuerdo que determina el precio de lista del medicamento en Suiza, un descuento y otras condiciones que rigen su inclusión en el sistema básico de seguro médico. La gran mayoría de estos modelos de precios son confidenciales. Esta práctica fue legalizada por el Parlamento Federal en 2025 como parte de la revisión de la LAMal, tras la presión del lobby farmacéutico.
Además de ser opaco, este sistema abre la puerta a un laberinto de acuerdos de reembolso, como ilustra el caso de Keytruda. En Suiza, el exitoso fármaco de MSD está sujeto a 26 modelos de precios con descuentos confidenciales, cada uno con condiciones que deben cumplirse para que esté cubierto por el sistema básico de seguro médico. Estas condiciones incluyen, por ejemplo, la aprobación previa de la aseguradora, restricciones vinculadas al tipo de cáncer, el plan de tratamiento y la naturaleza o duración del mismo.
Como resultado, el acceso a esta costosa terapia no está garantizado automáticamente. Sin embargo, el impacto financiero en los copagos de los pacientes y en el nivel de las primas de seguro que paga la población en general es muy real.
En Estados Unidos, un envase de 200 mg de Keytruda cuesta 11.760 dólares (9.300 francos suizos, precio de lista), lo que supone unos 200.000 dólares al año solo para este tratamiento. Al igual que en Suiza, en EE. UU. los pacientes deben pagar de su bolsillo un deducible elevado y copagos sustanciales, contribuyendo así a gran parte de los costes, o incluso a la totalidad si no tienen seguro médico. Esta situación puede acarrear graves dificultades económicas.
En cuanto a la India, una dosis estándar cuesta entre 1.750 y 2.000 francos suizos. En un país donde la mayoría de los pacientes pagan sus propios medicamentos, este precio resulta prohibitivo. Solo las personas más adineradas y con una cobertura de seguro suficiente pueden permitirse el tratamiento.
Proliferación de patentes
MSD puede mantener un precio elevado para Keytruda gracias a su exclusividad comercial, amparada en sus múltiples patentes primarias y secundarias (véase el recuadro).
Con el apoyo de la organización estadounidense sin ánimo de lucro I-MAK, reconstruimos el panorama de patentes del principio activo de Keytruda (pembrolizumab) en diversas jurisdicciones, utilizando bases de datos públicas. En total, identificamos 80 patentes concedidas a MSD en relación con esta molécula (véase el diagrama a continuación). Además, había 66 solicitudes de patente pendientes en Europa, 55 en Estados Unidos y 11 en India. Dada la dificultad de recopilar esta información, es posible que el número real de patentes que posee MSD para este tratamiento sea aún mayor.
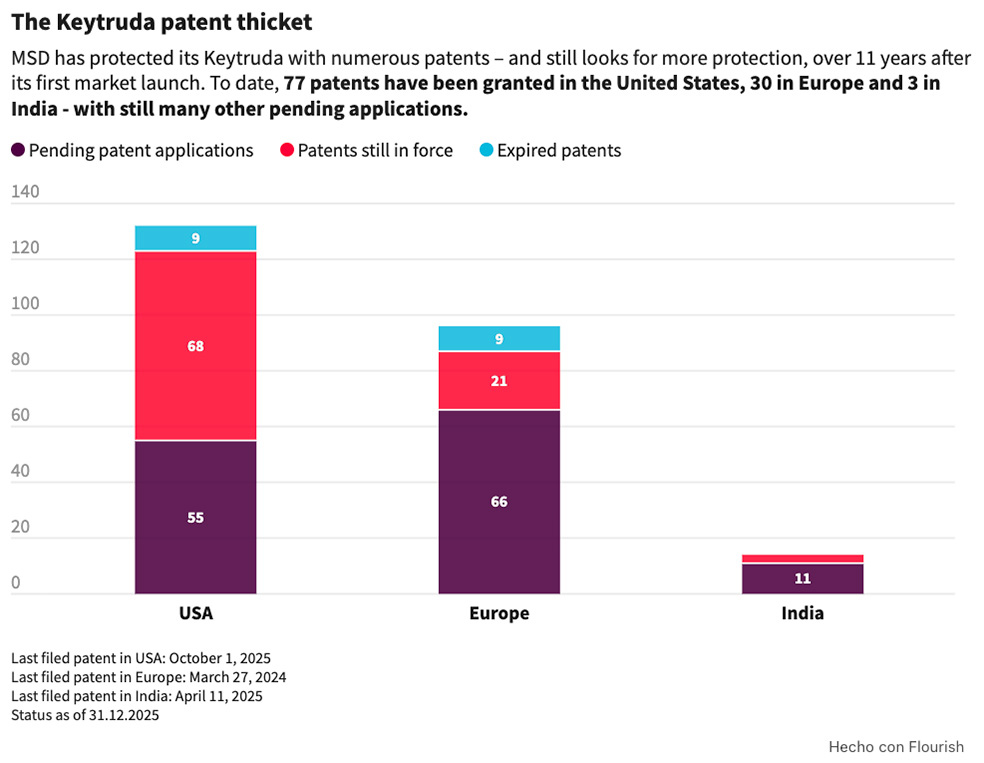
Este análisis nos permitió evaluar las consecuencias de estas patentes: otorgan a MSD un monopolio potencial de al menos tres décadas en Europa, India y Estados Unidos sobre la venta de este ingrediente activo tan demandado, lo que restringe el acceso al tratamiento. Esto supera con creces los 20 años previstos en el Acuerdo sobre los Aspectos de los Derechos de Propiedad Intelectual relacionados con el Comercio (ADPIC) de la Organización Mundial del Comercio.
En Suiza y Europa, gracias a una prórroga de la protección concedida por las autoridades nacionales, la exclusividad vinculada a la patente principal no expirará hasta 2031 (véase el gráfico a continuación). MSD se enfrentará a la competencia por primera vez en Estados Unidos e India en 2028, cuando expire la patente principal de Keytruda.
Alrededor de una docena de empresas están trabajando en versiones biosimilares de pembrolizumab (el equivalente biológico de los medicamentos genéricos), incluida la empresa suiza Sandoz. Estos fabricantes buscan hacerse con una parte de un mercado monumental: las ventas de Keytruda en Estados Unidos representan el 60 % de su facturación global, lo que supone un mercado valorado en casi 19.000 millones de dólares en 2025.
MSD amplía su monopolio
Hay mucho en juego financieramente, y MSD ya ha implementado contramedidas para extender su monopolio el mayor tiempo posible. En primer lugar, multiplicando las solicitudes de patentes secundarias, que representan aproximadamente el 95 % de sus títulos de protección, con una marcada aceleración en las solicitudes desde 2016, es decir, tras el lanzamiento de Keytruda. Posteriormente, modificando la vía de administración, pasando de la administración intravenosa a la inyección subcutánea. Esta táctica, denominada «cambio de producto», también utilizada por Roche y otras compañías farmacéuticas, permite obtener nuevas patentes secundarias y ampliar el nicho de exclusividad comercial en el mercado.
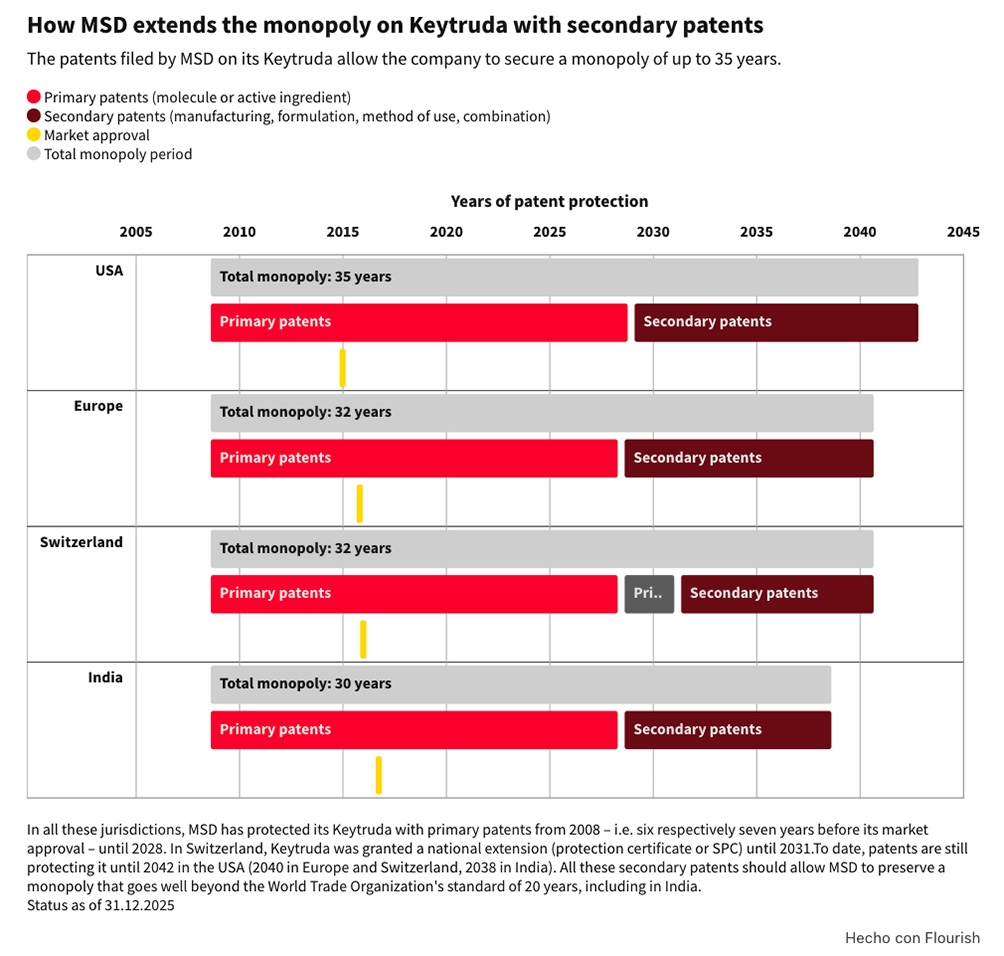
Según sus propias declaraciones, la compañía estadounidense planea cambiar entre el 30% y el 40% de su base de pacientes objetivo a la versión subcutánea de Keytruda —ya disponible en Estados Unidos y la UE, pero aún no en Suiza— para 2028. Con nuevas patentes que cubren esta vía de administración, podría extender su monopolio al menos hasta 2042.
Finalmente, el gigante estadounidense aún tiene la opción de iniciar acciones legales contra los fabricantes de biosimilares cuando estos se encuentran a punto de lanzar sus productos al mercado. El inicio de litigios también retrasa la entrada al mercado de biosimilares de la competencia.
Oficinas de patentes saturadas
Las patentes secundarias de MSD sobre pembrolizumab reivindican diversas modificaciones del producto, pero no cubren la sustancia activa, que permanece inalterada. Sobre todo, saturan las oficinas de patentes, prolongan la duración del monopolio y retrasan la competencia, sin exigir a cambio ningún beneficio terapéutico demostrado.
Conocida como «renovación indebida de patentes», la acumulación abusiva de patentes secundarias sobre productos terapéuticos es una práctica generalizada en la industria. En el caso de Keytruda, los competidores están impugnando la novedad de algunas de estas patentes. Una de ellas es Halozyme, una empresa especializada en este campo. La empresa biotecnológica argumenta que la versión subcutánea de Keytruda de MSD infringe 15 de sus patentes y ha emprendido acciones legales en Estados Unidos y Europa. Los procedimientos siguen en curso. En diciembre pasado, un tribunal alemán ordenó la prohibición de la comercialización de Keytruda subcutánea hasta que se resolviera el litigio.
La caja negra de los costos de I+D
¿Por qué un medicamento como Keytruda es tan caro? La industria farmacéutica argumenta repetidamente que sus tratamientos requieren grandes inversiones en investigación y desarrollo (I+D) y que las empresas deben asumir riesgos significativos de fracaso. Estos dos factores, según afirma, justifican los altos precios de los medicamentos una vez que llegan al mercado.
En su comparecencia ante el Comité de Salud del Senado de EE. UU. en febrero de 2024, el presidente y director ejecutivo de MSD declaró que su empresa había invertido 30 mil millones de dólares en el programa de investigación de Keytruda desde 2011. Esta cifra no se puede verificar, ya que las empresas no tienen la obligación de publicar ni contabilizar los costos de I+D de cada producto. Además, genera dudas, dado que MSD no participó en el descubrimiento ni en la concepción farmacológica del medicamento, que surgió en gran medida de investigaciones financiadas con fondos públicos. La empresa adquirió el tratamiento mediante una adquisición corporativa en 2009 e incluso consideró abandonarlo antes de cambiar de rumbo ante el éxito de un producto rival con un mecanismo de acción similar.
Para esclarecer este asunto, nos propusimos estimar las inversiones en I+D que MSD ha realizado hasta la fecha para Keytruda (Véase el gráfico en el formato original de Public Eye, reseñado al inicio).
Nuestra estimación de los costes de investigación y desarrollo de Keytruda asciende a 1.925 millones de dólares (1.520 millones de francos suizos), lo que equivale a tan solo el 1,2 % de las ventas mundiales del fármaco hasta la fecha. Esta cifra es muy inferior a la citada por el director ejecutivo de MSD. Incluso teniendo en cuenta los posibles fracasos, el coste total de la investigación y el desarrollo de Keytruda (4.790 millones de dólares, unos 3.800 millones de francos suizos) representa apenas el 3 % de la facturación del medicamento.
Con base en la metodología que desarrollamos, estimamos el margen de beneficio generado por MSD por las ventas de Keytruda en Suiza. Este margen representa más del 88 % del precio oficial
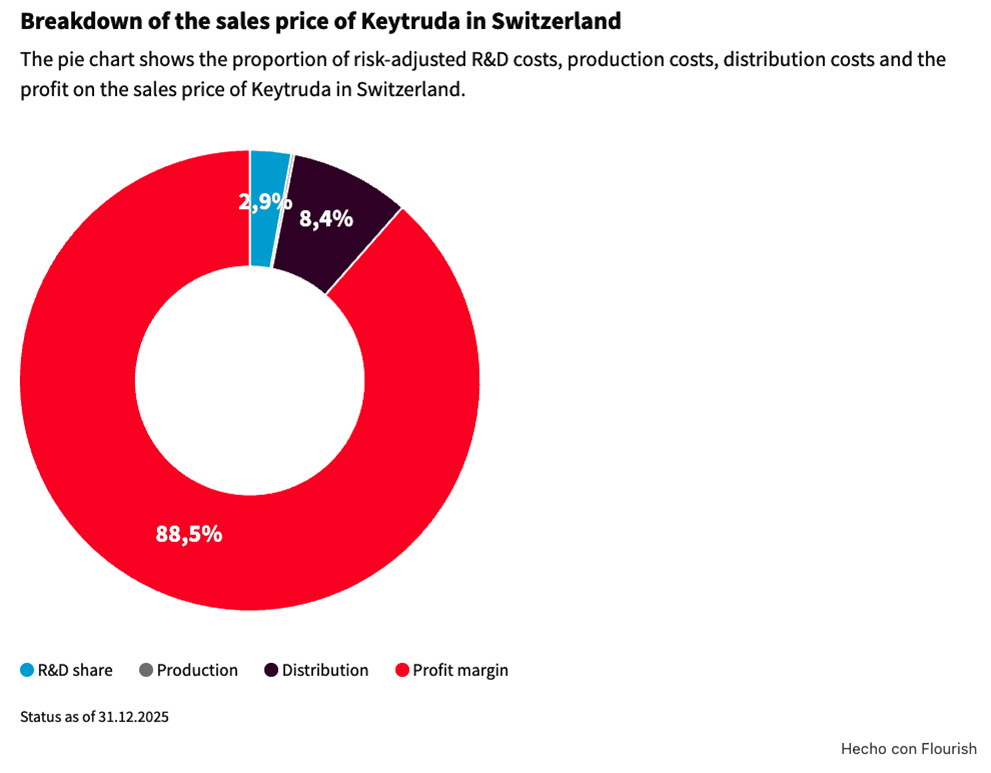
Este margen demuestra que las compañías farmacéuticas no utilizan precios elevados para compensar los considerables costes de I+D ni para mitigar riesgos, sino para generar beneficios exorbitantes. Lejos de reinvertirse sistemáticamente, estos beneficios ponen en entredicho el sistema de precios actual, que se supone que garantiza la sostenibilidad de la innovación.
Más transparencia, menos patentes
Los resultados de nuestra investigación sobre Keytruda subrayan una vez más la necesidad de actuar contra los precios excesivos de los medicamentos patentados. En Suiza, estos fármacos son uno de los principales factores del aumento de los costes sanitarios. El argumento esgrimido por las grandes farmacéuticas y la Casa Blanca —que los precios son demasiado bajos en Suiza y Europa— se contradice claramente con los considerables márgenes generados por empresas como MSD.
Las patentes otorgan a las farmacéuticas una posición de monopolio y una exclusividad comercial prolongada. Protegidas de la competencia, pueden imponer sus precios a nivel mundial, en detrimento de los pacientes y de los presupuestos de salud pública. Esto debe cambiar si queremos salvaguardar la sostenibilidad financiera de un sistema sanitario solidario que ahora se encuentra gravemente amenazado.
Es urgente que las autoridades de países con importantes corporaciones farmacéuticas, como Suiza, tomen medidas contra la proliferación abusiva de patentes secundarias sobre medicamentos. Como miembro del Convenio sobre la Patente Europea, Suiza podría exigir un escrutinio más riguroso de las solicitudes de patente para limitar su número.
Asimismo, deben reformarse los mecanismos de fijación de precios, exigiendo la divulgación de las inversiones reales realizadas por las empresas farmacéuticas y el porcentaje de financiación pública involucrada, en lugar de basarse en comparaciones internacionales de precios ineficaces.
En Suiza, los costes sanitarios son un problema creciente, y un número cada vez mayor de personas sufre el aumento desorbitado de las primas de los seguros. Las autoridades federales protegen un sistema que ayuda a las multinacionales a maximizar sus beneficios, impidiendo al mismo tiempo la realización del derecho a la salud para todos. Esta política también tiene repercusiones más allá de las fronteras suizas, ya que los precios de los medicamentos en Suiza se utilizan como referencia en más de 30 países, incluidos estados con economías más débiles. Al elevar los precios, Suiza no solo perjudica a su propia población, sino también a millones de pacientes en el extranjero.
¿Qué es una patente?
Una patente es un derecho exclusivo que permite al titular de una invención prohibir a terceros su fabricación y comercialización en los países donde se ha concedido la patente. Para ser patentable, una invención debe cumplir tres requisitos: ser nueva, implicar una actividad inventiva y ser susceptible de aplicación industrial. Por lo tanto, una modificación menor de un medicamento, incluso sin ningún beneficio terapéutico adicional, puede ser patentada.
En el sector farmacéutico se distinguen dos categorías de patentes: las patentes primarias protegen la molécula o moléculas del medicamento, mientras que las patentes secundarias están destinadas a proteger las modificaciones de productos ya patentados. En la práctica, estas últimas extienden artificialmente la duración de la exclusividad comercial.
El término «maraña de patentes» se utiliza cuando un medicamento está protegido por numerosas patentes. Si estas se solicitan durante un período prolongado, la duración del monopolio del producto puede superar con creces los 20 años previstos por el derecho internacional.