AUTOR: José Luis Rodríguez Agulló.
Ex-Jefe de Servicio de Digestivo. Hospital de Fuenlabrada.
Revista nº 11 de Abril de 2020.
Presentación
En la segunda mitad del siglo XX se descubrió que la hepatitis no-A no-B era un grave problema de salud porque era la causa más frecuente de inflamación crónica del hígado y cirrosis hepática. Pero no fue hasta 1989 cuando se descubrió el virus C y se demostró que la hepatitis no-A no B era causada por el virus C -la hepatitis C- (VHC).
Sin embargo, hasta 1991 no se dispuso en España y otros países de pruebas diagnósticas que pudiesen determinar la infección por el virus de la hepatitis C (VHC). El virus de la hepatitis C es un virus ARN para el que, basándose en la secuencia de nucleótidos y en el análisis filogenético, se han definido seis grupos mayores, llamados genotipos, designándose por números (genotipos 1 al 6) que se caracterizan por la sensibilidad diferente a los distintos tipos de tratamiento que se han utilizado en la etapa anterior.
La hepatitis C crónica (HCC) se consideraba como la primera causa de hepatitis postransfusional, de enfermedad hepática terminal, de indicación de trasplante (35%) y de carcinoma hepatocelular (CHC).
Hasta hace poco tiempo una citoquina, el interferón, aislado o en combinación con ribavirina, era el único tratamiento disponible para las hepatitis crónicas por el VHC, actuaban estimulando al sistema inmunológico para eliminar el virus e impidiendo la infección de otros hepatocitos en el caso de la ribavirina.
Los resultados obtenidos eran pobres por las múltiples contraindicaciones y efectos colaterales por lo que solo se podían tratar el 50% de los casos y, de estos, solo respondían un 25% que presentaban recaídas tardías, con lo que la tasa final de respuesta mantenida era de alrededor del 18-20%. El periodo de tratamiento era largo y los efectos colaterales incapacitantes casi universales. El interferón inhibe la replicación viral por mecanismos indirectos y reduce la necrosis hepática, la inflamación y la fibrosis.
Antivirales de acción directa
A partir de 2013 y años posteriores, el arsenal terapéutico contra el virus de la hepatitis C se amplió con los nuevos fármacos antivirales de acción directa (AAD), que impiden la replicación viral con efectos colaterales mínimos, son mucho más seguros, de administración oral y con una altísima eficacia, que permiten la curación del 98% de los pacientes. Con estos fármacos se puede incidir en tres fases del proceso replicativo del VHC: inhibiendo la proteasa viral, inhibiendo la polimerasa e inhibiendo la proteína NS5A.
Los tratamientos iniciales dependían de una combinación de varios y la duración del tratamiento del genotipo y tipo de lesión hepática. Según la fase del ciclo vital sobre la que actúan impidiendo la replicación del VHC reciben diferentes nombres agrupándolos por clases o familias de fármacos.
Identificamos tres familias disponibles [10]. Los nombres genéricos de los fármacos nos dan una pista si nos fijamos en su terminación:
1. Inhibidores de la proteasa: terminación en “previr”
2. Inhibidores de la polimerasa: terminación en “buvir”
3. Inhibidores de la proteína NS5A: terminación en “asvir”
Sin embargo, estos nuevos regímenes de AAD implican un incremento en el presupuesto de los sistemas de salud a corto plazo, debido al elevado coste de dichos fármacos y al aumento significativo de pacientes candidatos a recibir tratamiento por sus elevadas tasas de eficacia y excelente perfil de seguridad. Sin embargo, en lo positivo estos tratamientos implican una disminución en las necesidades de atención sanitaria: menos visitas médicas y de enfermería, menos analíticas y, por lo tanto, menos costes añadidos al coste del medicamento.
Los antivirales de acción directa fueron un gran avance en el tratamiento de la hepatitis C consiguiendo una eliminación del virus, respuesta viral sostenida, entre el 94 y el 98% de los casos dependiendo de la lesión hepática preexistente.
Antivirales de Acción Directa pangenotípicos
Un nuevo avance se produjo cuando se aprobaron a finales de 2017 los Antivirales de Acción Directa pangenotípicos que eran capaces de eliminar todos los genotipos del virus C. Como es necesario la combinación de 2 o 3 de estos fármacos los medicamentos actuales se presentan en una sola pastilla que incluye todos ellos.
Esta situación simplifica mucho el tratamiento porque su duración está establecida y ya no hay que elegir su tipo y la duración en función del genotipo e incluso se puede ampliar el espectro de los médicos que suministran y controlan el tratamiento. De forma general, no es imprescindible la determinación del genotipo del virus.
Algoritmo de tratamiento simplificado para VHC sin tratamiento previo y sin cirrosis o con cirrosis compensada. Recientemente se han publicado las recomendaciones de la American Association for the Study of Liver Diseases (AASLD) [11], coincidentes en lo esencial con las recomendaciones de la Asociación Europea para el Estudio del Hígado (EASL)[12] y también con las Australian recommendations for the management of hepatitis C virus infection: a consensus statement (June 2020)[13] .
Muchas de las recomendaciones incluidas en la última actualización de la guía sobre el VHC y que se destacan en este documento de la AASLD se ajustan y apoyan los objetivos de las estrategias de las Academias Nacionales de Ciencias, Ingeniería y Medicina (NASEM) y la OMS para pasar del control a la eventual eliminación de la hepatitis C. Entre los temas que se abordan están el cribado universal y el basado en el riesgo de la hepatitis C, los algoritmos de tratamiento simplificados para adultos sin tratamiento y sin cirrosis o con cirrosis compensada, el tratamiento de la hepatitis C en la población pediátrica, las pruebas y el tratamiento de la hepatitis C aguda y el trasplante de órganos de donantes con VHC a receptores con VHC negativo.
Varios estudios han comparado los regímenes de AAD entre sí. En general, cuando se da a elegir entre los regímenes recomendados de AAD contra el VHC, se prefiere el régimen menos costoso[14] por ser un uso más eficiente de los recursos, aunque alguno requiera la administración de varios comprimidos. Debido a la eficacia similar de la mayoría de los regímenes de AAD, el coste se convierte en el factor crítico que determina la rentabilidad relativa.
Los estudios también han calculado la rentabilidad del tratamiento del VHC en poblaciones especiales, como los pacientes en espera de un trasplante de hígado, los pacientes coinfectados por el VIH y el VHC, los que padecen una enfermedad renal crónica, las personas que se inyectan drogas y los adolescentes, todos ellos con ICER (ratio coste-eficacia incremental) favorables. En este momento, es razonable concluir que los regímenes de AAD proporcionan un buen valor para los recursos invertidos.

Ventajas de los AAD pangenotípicos
Simplifica mucho el tratamiento, porque las duraciones son estándar. No hay duraciones diferentes en función de las características de la enfermedad. Funcionan además en cualquier genotipo del virus. Anteriormente había que elegir el fármaco en función del genotipo.
Según destaca el propio Ministerio de Sanidad, estas nuevas terapias que bloquean la acción de proteínas esenciales para replicación del VHC son efectivas en un plazo de 8 a 12 semanas, presentan cuatro grandes ventajas sobre los tratamientos anteriores: simplifican el tratamiento; reducen las necesidades de seguimiento de los pacientes; aumentan las tasas de curación hasta cifras del 98%, algo impensable hasta ahora; y retrasan, en su caso, la aparición de complicaciones tardías y severas de la enfermedad.
La llegada de los tratamientos pangenotípicos ha supuesto un nuevo avance en el tratamiento de la hepatitis por el virus de la hepatitis C (VHC). Las mejoras introducidas por estas combinaciones de medicamentos han hecho que se actualicen las guías de tratamiento.
A finales de 2017 se aprobaron las combinaciones de sosfosbuvir/velpatasvir (Epclusa) y glecapravir/pibrentasvir (Mavyret), que sumados a elbasvir/grazoprevir (Zepatier) y ledipasvir/sofosbuvir (Harvoni), han puesto en manos del hepatólogo un arsenal terapéutico definitivo para tratar a cualquier paciente de hepatitis C, independientemente del genotipo y de la fase de la enfermedad.
Para los casos de fracaso, se aprobó a finales del pasado año la combinación de sofosbuvir (un inhibidor del nucleótido NS5B), velpatasvir (un inhibidor del NS5A) y voxilaprevir (un inhibidor del NS5A), comercializado como Vosevi, indicada para rescatar a estos pacientes. Su tasa de éxito asciende también a cifras que rondan el 98%.
La reciente aprobación y adopción de los antivirales de acción directa (AAD) pangenotípicos hizo necesaria una revisión de las directrices de la Organización Mundial de la Salud de 2015 para el tratamiento de las personas con infección por el virus de la hepatitis C (VHC)[15]. Según estas directrices y otras similares, la OMS publicó directrices actualizadas con una recomendación condicional, basada en pruebas de calidad moderada, para el uso de regímenes de AAD pangenotípicos para personas con infección crónica por el VHC de 18 años o más en julio de 2018.
Las intervenciones recomendadas en las guías de la OMS de julio de 2018 han demostrado una alta eficacia en todos los genotipos con perfiles de efectos colaterales escasos. La adopción generalizada de regímenes pangenotípicos para el tratamiento de la infección crónica por el VHC simplificará la administración y el tratamiento. Las administraciones orales sencillas y la corta duración del tratamiento mejorarán aún más la retención y la eficacia de los programas de salud pública. Esta nueva era de los AAD pangenotípicos es una adición bienvenida a la estrategia global de lucha contra la infección por el VHC.
El tratamiento simplificado con AAD pangenotípicos
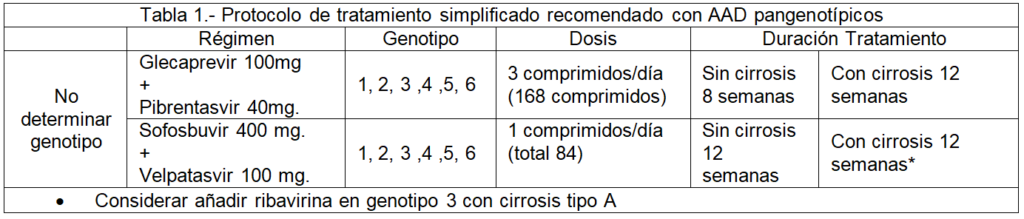
Los regímenes de tratamiento con AAD pangenotípicos ha dado lugar a la formulación de lo que ha dado en llamarse tratamiento simplificado de la hepatitis por VHC.
Las recomendaciones que establecen las guías de la American Association for Liver Diseases, European Association for the Study of the Liver y Australian recommendations for the management of hepatitis C virus infection: a consensus statement, para el tratamiento simplificado, sin genotipado/subtipado, de los pacientes adultos (>18 años) y adolescentes (12-17 años) que se aplica a pacientes infectados con VHC, son:
- Pacientes que nunca han recibido tratamiento para su infección por el VHC.
- Pacientes con hepatitis crónica C sin cirrosis o con cirrosis compensada (Child-Pough A).
- Pacientes tratados previamente con IFN pegilado y ribavirina; IFN pegilado, ribavirina y sofosbuvir; o sofosbuvir y ribavirina.
- Pacientes coinfectados con VIH.
El precio de los nuevos AAD pangenotípicos
El precio de los nuevos medicamentos es aprobado en la Comisión Interministerial de Precios de los Medicamentos (CPIMcuya composición está regulada en la disposición adicional primera del Real Decreto 485/2017, de 12 de mayo, por el que se desarrolla la estructura orgánica básica del Ministerio de Sanidad, Servicios Sociales e Igualdad (ahora Ministerio de Sanidad).
| Tabla 2.- Composición de la Comisión Interministerial de Precios de los Medicamentos |
| Presidencia: La persona titular de la Secretaría de Estado de Sanidad. |
| Vicepresidencia: La persona titular de la Dirección General de Cartera Básica de Servicios del Sistema Nacional de Salud y Farmacia. |
| Vocalías |
| 1.- Dos personas en representación del Ministerio de Economía y Empresa y Ministerio de Industria, Comercio y Turismo. |
| 2. Dos personas en representación del Ministerio de Hacienda. |
| 3. Tres representantes de las Comunidades Autónomas, a propuesta del Consejo Interterritorial del Sistema Nacional de Salud, elegidos entre sus miembros. |
| 4. La persona titular de la Subdirección General de Calidad de Medicamentos y Productos Sanitarios, de la Dirección General de Cartera Básica de Servicios del Sistema Nacional de Salud y Farmacia, que actuará como Secretario. |
| 5. Un funcionario de la Dirección General de Cartera Básica de Servicios del Sistema Nacional de Salud y Farmacia. |
| https://www.sanidad.gob.es/profesionales/farmacia/CIPMyPS.htm |
Los precios negociados de los medicamentos se consideran contratos comerciales confidenciales. Por lo tanto, casi no hay transparencia en cuanto a los precios reales pagados por los medicamentos contra la hepatitis C. Sin embargo, el descuento medio negociado a nivel internacional era del 22% en 2014 y en algunos casos ha aumentado al 46% al menos.
Con respecto a los precios en España no son accesibles por el público en general ni por los medios de comunicación. Recientemente, ante la exigencia del Consejo de Transparencia[16], el gobierno ha accedido a compartir el listado de precios. El movimiento se ha producido gracias a la campaña de No es Sano, que en abril de 2018 realizó una reclamación al Consejo de la Transparencia exigiendo la publicación de estos datos[17]. En su respuesta el Ministerio de Sanidad incluía los precios “legales” aprobados como se expresan en la Tabla 3.
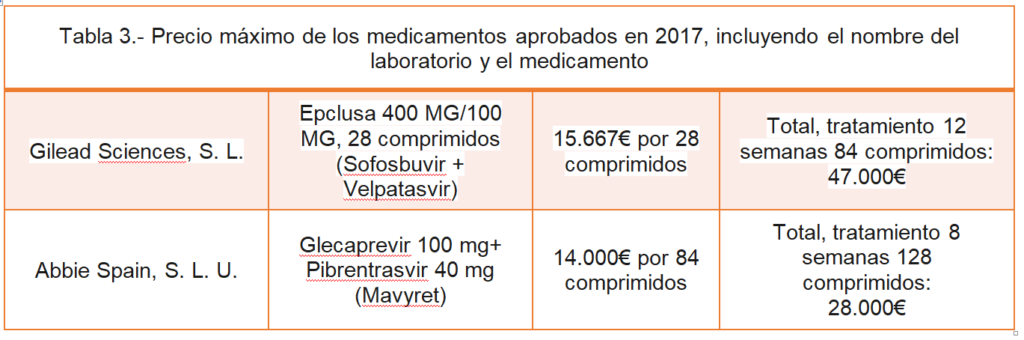
Podemos observar que el tratamiento con Glecaprevir + Pibrentrasvir, durante las 8 semanas establecidas, asciende a 28.000€ mientras que el tratamiento con Sofosbuvir + Velpatasvir, durante las 12 semanas establecidas, asciende a 47.000€.
“En general, cuando se da a elegir entre los regímenes recomendados de AAD contra el VHC, se prefiere el régimen menos costoso5 por ser un uso más eficiente de los recursos, aunque alguno requiera la administración de varios comprimidos”. Esta frase parece dedicada al mayor coste la combinación de Sofosbuvir + Velpatasvir en el tratamiento de la hepatitis crónica C.
Por otra parte, hay que comentar que en USA el tratamiento con Mavyret, Glecaprevir 100 mg + Pibrentrasvir 40 mg/3 comprimidos día/8 semanas, cuesta 26.000$9, es decir, 24.091,93 €, mientras que en España, con los precios aprobados por la Comisión Interministerial de Precios de los Medicamentos (CPIM), el precio ascendería a 28.000€, una incongruencia difícil de explicar. Además, en el caso Epclusa, Sofosbuvir 400 mg + Velpatasvir 100 mg, 1 comprimido durante 12 semanas, el precio ascendería a 47.000€ mientras que en USA costaría más, en concreto 75.000 dólares10, es decir, 69.528 € por 12 semanas.
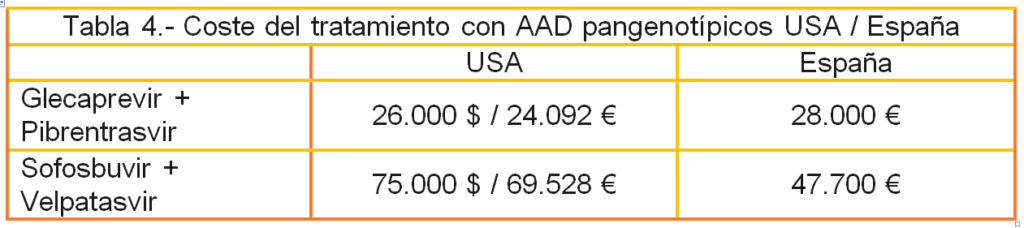
Especulando con la posibilidad de que se aplicase el “descuento medio negociado” del 22%”, el coste para el contribuyente de un tratamiento de hepatitis C con AAD pangenotípicos sería de 21.840 € para Glecaprevir + Pibrentrasvir y de 37.206 € para Sofosbuvir + Velpatasvir. Aunque aplicando el “descuento máximo negociado” del 46% un tratamiento con Glecaprevir + Pibrentrasvir costaría 12.880€ y un tratamiento con Sofosbuvir + Velpatasvir costaría 21.660 €.
Lo menos que se puede decir de esta situación es que es kafkiana, sobre todo cuando el gasto medio por paciente tratado de hepatitis C11 era de 9.473€ en septiembre de 2018. Las cifras no cuadran porque algo nos están ocultando, lo que demuestra la incongruencia de la política de medicamentos del Ministerio de Sanidad y la voracidad de las Big Pharma.
Como se puede leer en la página web de la Asociación Acceso Justo al Medicamento12:
“Estamos asistiendo en la actualidad a una presión insoportable de algunas compañías farmacéuticas, debido a su posición domínate en base a las patentes otorgadas por los gobiernos, que están rompiendo los equilibrios tradicionales al poner unos precios injustificados y abusivos. Esta presión está poniendo en riesgo la sostenibilidad de nuestro Sistema Nacional de Salud y obstaculizando el acceso de las poblaciones más vulnerables a los nuevos medicamentos. El Sistema Nacional de Salud tiene que detraer recursos de otras necesidades de atención sanitaria, del gasto en otro tipo de servicios y del gasto en remuneraciones del personal y de la incorporación de nuevos profesionales.
El abuso de la patente por parte de las compañías farmacéuticas al fijar precios altísimos y desproporcionados hace que la barrera de acceso sea el precio y no el coste. La dificultad de financiación de estos medicamentos no está en el coste de la fabricación, ni en el coste de la investigación, si no en el precio que ponen los fabricantes que llega a ser 20, 30 y más de 100 veces superior del coste de fabricación y de investigación.
El precio del medicamento debe cubrir el coste de producción y cubrir la inversión realizada en Investigación más Desarrollo, y permitir un beneficio razonable, que no debe exceder del 10%.”
Bibliografía:
- Fármacos disponibles para el tratamiento de la Hepatitis C. https://asscat-hepatitis.org/hepatitis-viricas/hepatitis-c/tratamiento-de-la-hepatitis-c/farmacos-disponibles-para-el-tratamiento-de-la-hepatitis-c/ consultado el 2 de abril de 2022
- HCV Guidance: Recommendations for Testing, Managing, and Treating Hepatitis C. https://www.hcvguidelines.org consultado el 2 de Abril de 2022.
- European Association for the Study of the Liver. EASL recommendations on treatment of hepatitis C: Final update of the series. Journal of Hepatology 2020 vol. 73 j 1170–1218.
- Australian recommendations for the management of hepatitis C virus infection: a consensus statement (June 2020). https://ashm.blob.core.windows.net/ashmpublic/hepatitis-C-virus-infection-a-consensus-statement-Jun-2020.pdf. Consultada el 18 de Abril de 2022
- Overview of Cost, Reimbursement, and Cost-Effectiveness Considerations for Hepatitis C Treatment Regimens. https://www.hcvguidelines.org/evaluate/cost. Consultada el 2 de abril de 2022.
- Michael J. Zoratti, Ayesha Siddiqua, Rita E. Morassut, Dena Zeraatkar, Roger Chou, Judith van Holten, Feng Xie, Eric Druyts. Pangenotypic direct acting antivirals for the treatment of chronic hepatitis C virus infection: A systematic literature review and meta-analysis. https://www.thelancet.com/journals/eclinm/article/PIIS2589-5370(19)30242-1/fulltext Published: January 05, 2020, DOI:https://doi.org/10.1016/j.eclinm.2019.12.007
- Consejo de Transparencia. Resolución 885/2019. Consejo Transparencia y Buen Gobierno. https://www.consejodetransparencia.es
- El gobierno publica los precios de los medicamentos financiados, pero sigue ocultando cómo los ha negociado con la industria. Diario.es 7 de noviembre 2018. https://www.eldiario.es/sociedad/precios-de-medicamentos-sanidad-farmaceuticas_1_1854196.html Consultado el 6 de abril de 2022.
- Glecaprevir/Pibrentasvir (Mavyret) for the Treatment of Chronic Hepatitis C. American Family Physicians. https://www.aafp.org/afp/2018/1115/p601.html Consultado el 10 de Abril 2022
- RANDI SOKOL, MD, MPH, MMedEd. Sofosbuvir/Velpatasvir (Epclusa) for Hepatitis C. Downloaded from American Family Physician website at www.aafp.org/afp Consultado el 10 de Abril 2022.
- Hepatitis C: el gasto por paciente se sitúa, desde 2015, en 18.000 euros, aunque ahora el SNS paga 9.700. DiarioFarma https://www.diariofarma.com/2018/11/02/hepatitis-c-desde-2015-el-gasto-medio-por-paciente-se-situa-en-18-000-euros-aunque-ahora-el-sns-paga-9-700 Consultado el 10 de Abril de 2022
- Asociación Acceso Justo al Medicamento https://accesojustomedicamento.org/quienes-somos/ Consultada el 20 de Abril de 2022
